
Wetenschap
Hoe lijkt silicium op koolstof?
1. Tetravalentie :Zowel silicium als koolstof zijn tetravalente elementen, wat betekent dat ze vier valentie-elektronen beschikbaar hebben voor binding. Door deze tetravalentie kunnen ze covalente bindingen vormen met andere atomen, waardoor een breed scala aan verbindingen ontstaat.
2. Vorming van covalente obligaties :Zowel silicium als koolstof vormen voornamelijk covalente bindingen door hun valentie-elektronen te delen. Deze eigenschap is fundamenteel voor de chemie van beide elementen en leidt tot de vorming van stabiele moleculaire structuren.
3. Verscheidenheid aan verbindingen :Silicium en koolstof staan bekend om hun vermogen om een breed scala aan verbindingen te vormen vanwege hun tetravalentie en veelzijdige bindingsmogelijkheden. Deze verbindingen omvatten organische verbindingen (in het geval van koolstof) en anorganische verbindingen (in het geval van silicium), zoals silicaten en siliciumcarbide.
4. Halfgeleidereigenschappen :Silicium en koolstof kunnen onder bepaalde omstandigheden beide halfgeleidend gedrag vertonen. Halfgeleiders zijn materialen met een elektrische geleidbaarheid die tussen die van geleiders en isolatoren ligt. Deze eigenschap maakt silicium en koolstof tot essentiële materialen op het gebied van de elektronica, vooral bij de productie van transistors en geïntegreerde schakelingen.
5. Kristalstructuren :Silicium en koolstof kunnen verschillende kristalstructuren vormen. Silicium kan bijvoorbeeld een diamantachtige kubieke kristalstructuur vormen, terwijl koolstof grafiet- en diamantstructuren kan vormen. Deze verschillende kristalstructuren zijn het resultaat van de verschillende rangschikkingen van atomen in het rooster en beïnvloeden de fysieke eigenschappen van de materialen.
6. Amorfe vormen :Zowel silicium als koolstof kunnen in amorfe vormen voorkomen, waarbij ze een goed gedefinieerde kristalstructuur missen. Amorf silicium en amorfe koolstof zijn belangrijke materialen in dunnefilmtechnologieën, zoals zonnecellen en elektronische beeldschermen.
Ondanks deze overeenkomsten hebben silicium en koolstof ook duidelijke verschillen in hun chemische gedrag en eigenschappen. Koolstof heeft bijvoorbeeld een lagere atomaire massa dan silicium, wat leidt tot verschillen in hun bindingsenergieën en chemische reactiviteit. Bovendien heeft silicium de neiging sterkere bindingen met zuurstof te vormen in vergelijking met koolstof, waardoor het beter bestand is tegen oxidatie. Deze verschillen resulteren in de verschillende kenmerken en toepassingen van materialen op basis van silicium en koolstof.
 Onderzoekers ontwikkelen sensoren die menselijke biomarkers en giftig gas detecteren
Onderzoekers ontwikkelen sensoren die menselijke biomarkers en giftig gas detecteren Wetenschappers maken gebruik van de superkracht van bloemen om de weg vrij te maken voor nieuwe medicijnbehandelingen
Wetenschappers maken gebruik van de superkracht van bloemen om de weg vrij te maken voor nieuwe medicijnbehandelingen  Is waterstofsulfide een covalente of ionische verbinding?
Is waterstofsulfide een covalente of ionische verbinding?  Hoe wordt water gevormd tijdens cellulaire ademhaling?
Hoe wordt water gevormd tijdens cellulaire ademhaling?  Bakstenen bouwen van plastic afval
Bakstenen bouwen van plastic afval
 Vijf kaarten die de resterende wildernis ter wereld onthullen
Vijf kaarten die de resterende wildernis ter wereld onthullen Uitlaatgas is de schuldige:ozon op leefniveau is schadelijk voor gewassen
Uitlaatgas is de schuldige:ozon op leefniveau is schadelijk voor gewassen Polsbandmonsters tonen vergelijkbare blootstelling aan chemische stoffen op drie continenten
Polsbandmonsters tonen vergelijkbare blootstelling aan chemische stoffen op drie continenten Klimaatverandering en duurzame levensstijl
Klimaatverandering en duurzame levensstijl Paleontologen ontdekken solide bewijs van voorheen ongrijpbare abrupte sprong op zeeniveau
Paleontologen ontdekken solide bewijs van voorheen ongrijpbare abrupte sprong op zeeniveau
Hoofdlijnen
- Machine learning toont verbanden tussen de groei van de bacteriële populatie en de omgeving
- Hoe wordt de kern van een cel gescheiden van het cytoplasma?
- Wat is het aantal chromosomen in een somatische cel?
- Welke van de volgende verklaringen verklaart het beste waarom soorten die zich seksueel voortplanten een voordeel hebben in een snel veranderende omgeving vergeleken met aseksueel?
- Onderzoek naar stekelbaarsvissen laat zien dat bij aanpassing aan nieuwe omgevingen veel genen betrokken zijn
- Nieuwe sorghumcultivars kunnen duizenden liters ethanol produceren
- Wat zijn de soorten gespecialiseerde cellen in planten?
- De reis van mangroven in Zuid-Japan volgen
- BESSY II werpt licht op hoe het interne kompas is opgebouwd in magnetotactische bacteriën
- Kunnen bezorgingen met drones het milieu helpen? Laten we dat uitpakken

- Student Hyperloop-motor getest bij ESA

- Regelgevers denken na:wanneer kunnen Boeings 737 MAX weer vliegen?

- Veilige solid-state lithiumbatterijen luiden paradigmaverschuiving in energieopslag in

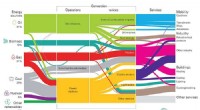
- Wereldwijde energiebesparingen aanpakken door efficiëntieverbeteringen
 Onderzoekers bieden een theoretische beschrijving van topologische watergolfstructuren
Onderzoekers bieden een theoretische beschrijving van topologische watergolfstructuren  Wat is kaviaar? Oorsprong, typen en productie
Wat is kaviaar? Oorsprong, typen en productie  Als school thuis is en thuis school, welke regels prevaleren?
Als school thuis is en thuis school, welke regels prevaleren? Samsung stelt lancering nieuw Galaxy-apparaat vast voor oktober
Samsung stelt lancering nieuw Galaxy-apparaat vast voor oktober Science Fair Project: Growing Crystals
Science Fair Project: Growing Crystals Tests tonen een mooie toekomst voor gadonanobuisjes bij het volgen van stamcellen
Tests tonen een mooie toekomst voor gadonanobuisjes bij het volgen van stamcellen Maillardets Automaton is een wonder van de 19e-eeuwse robotica
Maillardets Automaton is een wonder van de 19e-eeuwse robotica  Taiwans schubdieren lijden een golf van aanvallen van wilde honden
Taiwans schubdieren lijden een golf van aanvallen van wilde honden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

