
Wetenschap
Hoe temperatuur de overgang tussen vast, vloeibaar en gas drijft
Door Matthew Perdue Bijgewerkt op 24 maart 2022
showcake/iStock/Getty Images
Temperatuur weerspiegelt de gemiddelde kinetische energie van de moleculen waaruit een stof bestaat. Of je het nu in Celsius, Fahrenheit of Kelvin meet, de temperatuur bepaalt hoe deze moleculen bewegen en op elkaar inwerken, en bepaalt uiteindelijk de toestand van de materie.
Het vries- of smeltpunt
De moleculen van een vaste stof zitten in een dicht opeengepakte, geordende opstelling, waardoor het materiaal een stijve vorm krijgt die bestand is tegen verandering. Naarmate de temperatuur stijgt, trillen de moleculen krachtiger, waardoor de krachten die ze bij elkaar houden worden verzwakt. Wanneer de trillingsenergie het smeltpunt van de vaste stof bereikt, valt de structuur uiteen en verandert de vaste stof in een vloeistof. Omgekeerd zorgt het afkoelen van een vloeistof tot onder dezelfde temperatuur ervoor dat deze weer bevriest tot een vaste stof. Daarom is het smeltpunt ook het vriespunt.
Het kook- of condensatiepunt
Vloeistoffen laten hun moleculen langs elkaar bewegen, waardoor de substantie de vorm van de container aanneemt. Het verhogen van de temperatuur voegt kinetische energie toe, waardoor de moleculen sneller gaan trillen. Zodra ze het kookpunt bereiken, is de energie voldoende om moleculen in de lucht te laten ontsnappen, waardoor de vloeistof in een gas wordt omgezet. Wanneer een gas tot onder deze drempel wordt afgekoeld, verliezen de moleculen energie, botsen ze vaker en condenseren ze weer tot een vloeistof op het condensatiepunt.
Kinetische energie van gassen
Gassen bezitten de hoogste kinetische energie van de drie toestanden van materie, en ze bestaan bij de hoogste temperaturen. In een open systeem verspreidt het verhogen van de temperatuur de gasmoleculen alleen maar verder uit elkaar; de staat blijft gas. In een gesloten container botsen de sneller bewegende moleculen echter vaker tegen de wanden, waardoor de druk toeneemt. Deze relatie tussen temperatuur en druk vormt de basis van veel technische en wetenschappelijke toepassingen.
Effect van druk en temperatuur
Druk is een andere kritische factor die samenwerkt met de temperatuur om de toestand van de materie te bepalen. Volgens de wet van Boyle zijn temperatuur en druk recht evenredig:een stijging van de temperatuur leidt tot een stijging van de druk. Bij voldoende lage drukken en temperaturen kan een vaste stof de vloeibare fase helemaal overslaan en direct overgaan in een gas door middel van sublimatie, een fenomeen dat voorkomt bij droogijs en sneeuw.
 Onderzoekers onderzoeken hulpbronnenschaarste en armoedevallen in de kust van Tanzania
Onderzoekers onderzoeken hulpbronnenschaarste en armoedevallen in de kust van Tanzania Wat is het verschil tussen hardhout en zachthout?
Wat is het verschil tussen hardhout en zachthout?  "Cold Desert Biome Plants
"Cold Desert Biome Plants Onderzoek naar orkaanschade zal waarschijnlijk wereldwijd helpen
Onderzoek naar orkaanschade zal waarschijnlijk wereldwijd helpen Honger, droogte, ziekte:VN-klimaatrapport onthult ernstige bedreigingen voor de gezondheid
Honger, droogte, ziekte:VN-klimaatrapport onthult ernstige bedreigingen voor de gezondheid
Hoofdlijnen
- Zeepaardjesvaders bevallen op een unieke manier, blijkt uit nieuw onderzoek
- Niet zo koude eend? Man blijft zoeken naar uitgestorven vogel
- Welke wetenschapper toonde aan dat planten zuurstof produceren?
- Welke cellen omringen en vernietigen bacteriën?
- Zijn kwallenleden van de cnidarian -klasse?
- Welke intraveneuze oplossingen zullen hoogstwaarschijnlijk de groei van micro -organismen bevorderen?
- Wat zijn drie vormen van monosachariden?
- Over wetenschapper en kenmerkend voor wetenschapper?
- Wat is de algemene vorm van een plantencel?
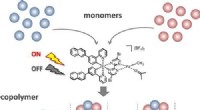
- Aangepaste sequenties voor polymeren die zichtbaar licht gebruiken
- Onderzoekers onthullen reactieve galliumhydridesoorten op galliumoxideoppervlak

- Biochemici onthullen hoe complexe moleculen ijzer door het lichaam verplaatsen

- Heteractis magnifica zeeanemonen kunnen helpen bij het bestrijden van de ziekte van Alzheimer

- Bestrijding van kunstmatige trilhaartjes met magnetische velden en licht

 De naam van het zuur dat in oranje aanwezig is?
De naam van het zuur dat in oranje aanwezig is?  Is kwik groter dan de maan?
Is kwik groter dan de maan?  E.coli een toekomstige energiebron?
E.coli een toekomstige energiebron?  Hondsdolheid bij eekhoorns:de belangrijkste tekenen en symptomen herkennen
Hondsdolheid bij eekhoorns:de belangrijkste tekenen en symptomen herkennen  Tijdens actieve transportstoffen komen van regio's van wat?
Tijdens actieve transportstoffen komen van regio's van wat?  Maken producenten voedsel van kooldioxide water en energie de zon?
Maken producenten voedsel van kooldioxide water en energie de zon?  Hoe sociale media antisemitisme aanwakkeren
Hoe sociale media antisemitisme aanwakkeren Wat gebeurt er met aardmaterialen tijdens depositie?
Wat gebeurt er met aardmaterialen tijdens depositie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

