
Wetenschap
Drie belangrijke eigenschappen van ionische verbindingen
Door Drew Lichtenstein Bijgewerkt op 24 maart 2022
Een verbinding is een stof die wordt gevormd door het combineren van twee of meer verschillende atomen. Wanneer deze atomen bij elkaar worden gehouden door de elektrostatische aantrekkingskracht tussen tegengesteld geladen ionen, is het resulterende materiaal een ionische verbinding.
Definitie
Ionische verbindingen bestaan uit ten minste één metaal en één niet-metaal. Een ion wordt gevormd wanneer een atoom elektronen verliest of wint, waardoor een positieve of negatieve lading ontstaat. De ionische binding zorgt voor een krachtige aantrekkingskracht tussen deze geladen soorten.
Solid State bij kamertemperatuur
Door hun sterke ionische bindingen zijn deze materialen onder normale omstandigheden vast. Ze vertonen een stijve roosterstructuur, die verantwoordelijk is voor hun hoge smelt- en kookpunten. Een bekend voorbeeld is keukenzout (NaCl), dat kristalliseert tot een kubisch rooster van Na⁺- en Cl⁻-ionen. Hoewel ionische verbindingen vaak oplosbaar zijn in water, verandert de oplosbaarheid hun vaste toestand niet.
Metaalkenmerken
Veel ionische vaste stoffen vertonen metaalachtige eigenschappen:ze reflecteren licht (glans), hebben een hoge dichtheid en geleiden warmte en elektriciteit wanneer ze gesmolten of opgelost zijn, hoewel hun geleidbaarheid in vaste toestand relatief laag is.
Stabiele ionische bindingen en thermische eigenschappen
De energie die ionen in het rooster bij elkaar houdt, wordt roosterenergie genoemd. Deze robuuste binding maakt ionische verbindingen bestand tegen verandering, wat resulteert in smeltpunten die enkele honderden graden Celsius kunnen bereiken en kookpunten ver boven die van covalente moleculen.
Het begrijpen van deze eigenschappen (vaste structuur, metaalachtige eigenschappen en sterke ionische binding) geeft inzicht in waarom ionische verbindingen zich gedragen zoals ze dat doen in de dagelijkse chemie.
 Behoort boor tot de metaalfamilie?
Behoort boor tot de metaalfamilie?  Het roosteren van cacaobonen kan zowel de gezondheidsvoordelen van chocolade behouden, smaak
Het roosteren van cacaobonen kan zowel de gezondheidsvoordelen van chocolade behouden, smaak Astatine Een radioactief lid van de halogeenfamilie vormt zich samen met waterstof voorspellen zijn chemische formule?
Astatine Een radioactief lid van de halogeenfamilie vormt zich samen met waterstof voorspellen zijn chemische formule?  Wat is het volume van 1 liter water in damp?
Wat is het volume van 1 liter water in damp?  Wat zijn enkele interessante feiten over melkzuur?
Wat zijn enkele interessante feiten over melkzuur?
 Bacteriën die worden gebruikt om met diesel vervuilde grond in Groenland schoon te maken
Bacteriën die worden gebruikt om met diesel vervuilde grond in Groenland schoon te maken Hoe vis voedsel verkrijgen?
Hoe vis voedsel verkrijgen?  Welke plaats ter wereld ontvangt de meeste zure regen?
Welke plaats ter wereld ontvangt de meeste zure regen?  Wat ben je de laatste fase van aquatische opvolging?
Wat ben je de laatste fase van aquatische opvolging?  Hoe mossen en het klimaat het lot van stikstof in het Boreale gebied bepalen
Hoe mossen en het klimaat het lot van stikstof in het Boreale gebied bepalen
Hoofdlijnen
- Welke twee levensdomeinen bestaan prokaryoten?
- Hoe zijn wortels verschillende rhizoïden?
- Dugongs zullen waarschijnlijk functioneel uitgestorven zijn in China
- Welke twee factoren bepalen een bioom?
- Naar welk deel van de cel transcriptiereizen doen?
- Overleving van dierlijke cellen:sleutelprocessen en opname van voedingsstoffen
- Wat is de term die vrij betekent van microben in het menselijk lichaam?
- Natuurkundigen modelleren de vouwing van chromosomen en onthullen hoe lussen de ruimtelijke organisatie van het genoom beïnvloeden
- Wat is een voorbeeld van intern en extern in wetenschapsdefinities?
- Nieuw rekenmodel van chemische bouwstenen kan de oorsprong van het leven helpen verklaren

- Video:Wat is octaan eigenlijk?

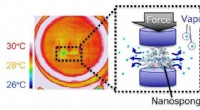
- Ontwikkeling van een nieuw type koeling via gedwongen overgang naar vloeibaar gas
- Onderzoek onthult meer over het pad dat bacteriële ziekteverwekkers afleggen om tuberculose te veroorzaken

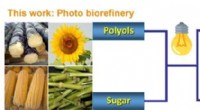
- Nieuwe fotokatalytische methode zet biopolyolen en suikers om in methanol en syngas
 Is Saturnus een gasreus of rotsachtig?
Is Saturnus een gasreus of rotsachtig?  Kunnen techreuzen samenwerken tegen hun gemeenschappelijke vijanden?
Kunnen techreuzen samenwerken tegen hun gemeenschappelijke vijanden? Alle abiotische en biotische factoren in een kleine bosvormen?
Alle abiotische en biotische factoren in een kleine bosvormen?  lichtgewicht, slagvaste honingraatstructuren kunnen voelen wanneer ze beschadigd zijn
lichtgewicht, slagvaste honingraatstructuren kunnen voelen wanneer ze beschadigd zijn Het opzetten van een systeem voor 911 videobellen brengt ontwerpuitdagingen met zich mee
Het opzetten van een systeem voor 911 videobellen brengt ontwerpuitdagingen met zich mee Waar gaat Biochemistry over?
Waar gaat Biochemistry over?  Onderzoeken waarom partijen in conflict ophouden met vechten
Onderzoeken waarom partijen in conflict ophouden met vechten  Wat is de betekenis van insturacties?
Wat is de betekenis van insturacties?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

