
Wetenschap
Molariteit beheersen:een stapsgewijze handleiding voor het berekenen van initiële concentraties
Molariteit beheersen:een stapsgewijze handleiding voor het berekenen van initiële concentraties
Door bijdragende schrijver • Bijgewerkt op 24 maart 2022
Het berekenen van de initiële concentratie van een oplossing, gewoonlijk molariteit genoemd, is een fundamentele vaardigheid in de chemie en biochemie. Molariteit drukt uit hoeveel mol opgeloste stof aanwezig is per liter oplossing.
Stap 1:Zet de massa van de opgeloste stof om in mol
Weeg de opgeloste stof in grammen en deel deze vervolgens door de molaire massa. Natriumhydroxide (NaOH) heeft bijvoorbeeld een molaire massa van 40,0 gmol⁻¹. Als je 20,0 g NaOH oplost:
molNaOH = 20,0 g × (1mol / 40,0 g) = 0,50 mol
Stap 2:Bepaal het volume oplosmiddel in liters
Meet het oplosmiddelvolume. Als de meting in milliliters is, reken dan om naar liters (1L =1000 ml). 500 ml oplosmiddel is bijvoorbeeld gelijk aan:
500 ml × (1 l / 1000 ml) =0,500 l
Stap 3:Bereken de molariteit
Verdeel het aantal mol opgeloste stof door het volume oplosmiddel in liters:
M = 0,50mol / 0,500L = 1,0MNaOH
De oplossing heeft dus een molariteit van 1 M. Het verhogen van het oplosmiddelvolume zou de molariteit verlagen, terwijl het verlagen ervan de concentratie zou verhogen.
TL;DR (te lang; niet gelezen)
Houd de eenheden tijdens de hele berekening bij:converteer gram naar mol en milliliter naar liter, om conversiefouten te voorkomen bij het bepalen van de molariteit.
 Leg de functies van oplossing A en B uit?
Leg de functies van oplossing A en B uit?  Is de verdamping van water uit de suikeroplossing een fysische of chemische verandering?
Is de verdamping van water uit de suikeroplossing een fysische of chemische verandering?  Wat doen atomen en moleculen voortdurend?
Wat doen atomen en moleculen voortdurend?  Welk volume waterstof bij STP wordt geproduceerd uit de reactie 50,0 g mg en equivalent 75 HCl?
Welk volume waterstof bij STP wordt geproduceerd uit de reactie 50,0 g mg en equivalent 75 HCl?  Chemici ontdekken sleutel tot groenere voedselproductie
Chemici ontdekken sleutel tot groenere voedselproductie
Hoofdlijnen
- Is en Lionfish Carnivore Orherbivore of Omnivore?
- Hoe worden overeenkomsten in macromoleculen tussen organismen die als bewijs worden gebruikt om de evolutie te ondersteunen?
- Hoe is Sporozoans belangrijk voor mensen?
- Een RNA TREAT voor Halloween
- Wat is positieve psychologie?
- Waarom heeft de evolutie ons niet het vermogen gegeven om zoet water te ruiken?
- Waarom is osmose belangrijk in het menselijke lichaam?
- Wat zijn de drie componenten van een celmembraan?
- Een lange opgerolde buis waarin voedsel wordt verteerd en geabsorbeerd?
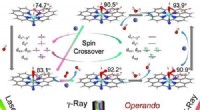
- Wetenschappers identificeren elektronische en structurele dynamiek van katalytische centra in materialen met één Fe-atoom
- 3D-printen van zetmeel voor gepersonaliseerde medicijnontwikkeling

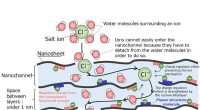
- Zeer functioneel membraan ontwikkeld voor de productie van zoetwater uit zeewater
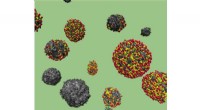
- Synthesestudies transformeren afvalsuiker voor toepassingen voor duurzame energieopslag
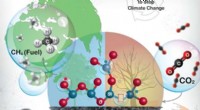
- De koolstofkringloop sluiten om klimaatverandering te stoppen
 Wordt energie vrijgegeven wanneer waterdamp in vloeistof condenseert?
Wordt energie vrijgegeven wanneer waterdamp in vloeistof condenseert?  Welk mobiele telefoonsbedrijf biedt de gratis onbeperkte oproepen tussen 2 telefoons?
Welk mobiele telefoonsbedrijf biedt de gratis onbeperkte oproepen tussen 2 telefoons?  Wat is een biologisch exemplaar?
Wat is een biologisch exemplaar?  Hoe brandweerwagens werken
Hoe brandweerwagens werken  Wat is de chemische formule voor calciumperchloraat?
Wat is de chemische formule voor calciumperchloraat?  Scheiding van waterstof en koolmonoxide:methoden en efficiëntie
Scheiding van waterstof en koolmonoxide:methoden en efficiëntie  Verschil tussen voorjaarsschaal & straalscala
Verschil tussen voorjaarsschaal & straalscala  Wat zijn drie dingen die kunnen gebeuren om te zwaaien terwijl het door verschillende materialen beweegt?
Wat zijn drie dingen die kunnen gebeuren om te zwaaien terwijl het door verschillende materialen beweegt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

