
Wetenschap
Chemici ontdekken sleutel tot groenere voedselproductie

Door blauw licht op iridium te laten schijnen, wordt het "opgewonden, ” waardoor het de energie krijgt om tegen het antraceenmolecuul te botsen en een waterstofatoom over te brengen, het maken van een zwakke band. De iridiumkatalysator activeert vervolgens waterstofgas, het voltooien van de cyclus. Krediet:Princeton University
Misschien wel de belangrijkste (zo minst bekende) industriële vooruitgang van de 20e eeuw, het Haber-Bosch ammoniaksyntheseproces overwon in wezen voedselschaarste door de middelen te creëren voor massaproductie van kunstmest - kunstmest die vervolgens werd gebruikt om voedseloogsten over de hele wereld te versterken.
Maar de productie van ammoniak - de bouwsteen voor ammoniumnitraatmeststof - genereert een problematisch bijproduct langs de lijn:koolstofdioxide. Veel:meer dan twee ton koolstof voor elke ton kunstmest. Het is goed voor naar schatting 1,4% van de wereldwijde uitstoot van kooldioxide. Dus, terwijl het proces massale hongersnood tegenging, het begon ook de last van broeikasgassen van de planeet op te voeren.
Een van de belangrijkste doelen voor wetenschappers vandaag is het loskoppelen van de voedselproductie van koolstof. Gedeeltelijk, dit betekent een manier vinden om kunstmest te produceren door middel van koolstofvrije ammoniaksynthese. Kan het zonder Haber-Bosch?
Paul Chirik, de Edwards S. Sanford hoogleraar scheikunde, heeft een belangrijke stap gezet in de richting van deze mogelijkheid met een unieke, fundamentele benadering van de synthese van chemische bindingen. Hij en de onderzoekers in zijn lab gebruiken zichtbaar licht om de vorming van zwakke element-waterstofbindingen te stimuleren. die de kern van de uitdaging vormen omdat ze zo moeilijk te maken zijn.
Het proof-of-concept paper van het lab, deze maand gepubliceerd in Natuurchemie , legt een eenvoudige methode uit waarbij blauw licht op een iridiumkatalysator schijnt om de vorming van zwakke bindingen op of in de buurt van thermodynamisch potentieel mogelijk te maken, dat wil zeggen, zonder enorme energie-uitgaven - zonder een koolstofbijproduct.
"De grote doorbraak hier is de mogelijkheid om licht te nemen en dan een chemische reactie te bevorderen om een echt zwakke binding te maken, dat je niet zonder een externe prikkel zou kunnen, "zei Chirik. "In het verleden, die stimulans is gekoppeld aan het maken van afval of het verbruik van elektriciteit. Hier, we doen het met licht.
"We hebben deze wereld van metaalkatalysatoren die verbazingwekkende dingen hebben gedaan - ze hebben ammoniak gemaakt, ze hebben drugs gemaakt, ze hebben polymeren gemaakt. Nutsvoorzieningen, we kunnen er nog meer mee doen als we gaan kijken wat er gebeurt als deze katalysatoren licht absorberen, "voegde hij eraan toe. "Dus, je neemt iets dat voorheen echt coole chemie deed en je maakt er sap van met nog eens 50 kilocalorieën.
"Er gaat een hele wereld open. Plotseling, er is een nieuwe klasse van reacties die we kunnen bedenken om te doen."
Schijn een licht
E-H-bindingen zijn gewoon een manier om eventuele bindingen aan te duiden die je zou kunnen maken tussen waterstof en een ander element. E-H-bindingssterkten zijn sterk afhankelijk van de chemische structuur van elk element, maar veel van deze bindingen zijn zwak - instabiel en geneigd om gemakkelijk te breken en waterstof te vormen (H 2 ). De meeste chemische reacties worden aangedreven door de vorming van sterke bindingen, omdat er energie vrijkomt wanneer stabielere producten worden gevormd. Het is de assemblage van zwakke bindingen die de uitdaging vormt.
Het Chirik-lab heeft een manier gevonden om een zwakke binding te maken door licht op een katalysator te laten schijnen; in dit geval, iridium.
Zo werkt het:onderzoekers kozen een representatief organisch molecuul, antraceen, die fungeert als een soort platform waarop de chemie plaatsvindt in de reactiekolf. Door blauw licht op iridium in de fles te laten schijnen, wordt het "opgewonden, " wat betekent dat het energie heeft om de reactie aan te drijven. In deze toestand, het botst tegen het antraceenmolecuul en brengt een waterstofatoom over om een zwakke binding te maken. De iridiumkatalysator activeert vervolgens waterstofgas, het voltooien van de cyclus.
Het gebruik van waterstofgas in plaats van op koolstof gebaseerde waterstofbronnen - in het verleden veel gebruikt in organische synthese - biedt mogelijk een duurzame manier om zwakke chemische bindingen te maken zonder een koolstofbijproduct te genereren.
Yoonsu-park, een postdoctoraal onderzoeksmedewerker in het laboratorium van Chirik en hoofdauteur van het papier, en Sangmin Kim, een doctoraat in 2021 afgestudeerd aan het laboratorium, kwam op het idee om fotochemie te gebruiken door zwakke bindingen te bekijken die in andere reacties voorkomen en hun lessen te extrapoleren. Twee extra auteurs op het papier - Greg Scholes, de William S. Tod hoogleraar scheikunde, en zijn afgestudeerde student Lei Tian— droegen inzichten bij in de rol van blauw licht met behulp van een verscheidenheid aan laserexperimenten.
Park bepaalde ook welke metaalkatalysator in de enorme uitgestrektheid van het periodiek systeem het meest effectief zou zijn in het uitvoeren van de gewenste reactie. Afstappen van eerder laboratoriumwerk gedaan met rhodium - nog een zeldzame, dure metaalkatalysator - hij richtte zich snel op iridium.
Hoewel wetenschappers nog niet klaar zijn om Haber-Bosch overboord te zetten, de proof-of-concept van het Chirik-lab is een belangrijke eerste stap.
"We hebben ammoniak nog niet katalytisch gemaakt. We hebben nog een lange weg te gaan om dat doel te bereiken, " zei Chirik. "Maar het is dit idee om te leren hoe je deze zwakke banden kunt maken dat zo belangrijk is.
"Wat ik leuk vind aan dit onderzoek is, het is anders. Het is fundamentele chemie, zo eenvoudig als je kunt krijgen. Niemand opent morgen een fabriek voor dit onderzoek. Maar we zijn erg enthousiast over het concept, en we hopen echt dat andere mensen deze chemie in andere contexten doen."
 Feiten over de Colorado-rivier
Feiten over de Colorado-rivier  grondwater, een bedreigde hulpbron die duurzaam beheer vereist
grondwater, een bedreigde hulpbron die duurzaam beheer vereist Zijn natuurlijke vezels echt beter voor het milieu dan microplastic vezels?
Zijn natuurlijke vezels echt beter voor het milieu dan microplastic vezels? NASA vindt kleine overblijfselen van tropische cycloon Owen
NASA vindt kleine overblijfselen van tropische cycloon Owen Waarschuwingssysteem heeft mogelijk levens gered in Indonesische tsunami
Waarschuwingssysteem heeft mogelijk levens gered in Indonesische tsunami
Hoofdlijnen
- Wat zijn de primaire functies van fosfolipiden?
- Wat wordt er gebruikt om DNA op een specifieke locatie voor splitsing te knippen?
- Wat is de complementaire basispaarregel?
- Rollen van celorganellen in mitose
- Wat zijn de vier stikstofbasen van DNA?
- Beperkingen van enzymen gebruikt in Forensic Science
- Cilia: definitie, types en functie
- Wat is een prehistorische toolkit en hoe zou het de menselijke geschiedenis kunnen herschrijven?
- Welke genen en genomen onthullen over onze gezondheid
- Forensisch chemicus gebruikt zweet om personen op plaats delict te onderscheiden

- Onderzoeksgroep vindt manier om plastic afvalproducten om te zetten in vliegtuigbrandstof

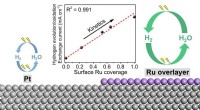
- Nieuwe mechanismen voor verbetering van de activiteit van bimetaalkatalysatoren voor waterstofopwekking en brandstofcellen
- Onderzoekers patenteren snelle tests voor cocaïne

- Medische zuurstof mag geen luxe zijn:een goedkopere manier ontwikkelen om het te produceren

 Tiener klimaatactivist tegen Franse critici:luister naar de wetenschap
Tiener klimaatactivist tegen Franse critici:luister naar de wetenschap Wat betekent gegevens in een wetenschapsbeursproject?
Wat betekent gegevens in een wetenschapsbeursproject?  Een litteken dat de Woolsey Fire achterliet
Een litteken dat de Woolsey Fire achterliet NASA volgt tropische storm Soulik in de Zee van Japan
NASA volgt tropische storm Soulik in de Zee van Japan Onderzoekers lossen wetenschappelijke puzzel op die de efficiëntie van zonnepanelen kan verbeteren
Onderzoekers lossen wetenschappelijke puzzel op die de efficiëntie van zonnepanelen kan verbeteren Japans geroemde waarschuwingssysteem loopt tegen limieten aan
Japans geroemde waarschuwingssysteem loopt tegen limieten aan De jacht op de ruimte begint terwijl de Binar-1-missie van West-Australië de volgende grote sprong maakt
De jacht op de ruimte begint terwijl de Binar-1-missie van West-Australië de volgende grote sprong maakt Video:hoe traangas je lichaam beïnvloedt
Video:hoe traangas je lichaam beïnvloedt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

