
Wetenschap
Waarom fenolftaleïne van kleur verandert:de wetenschap achter zuur-base-detectie
Door Rosann Kozlowski, bijgewerkt op 30 augustus 2022
Dick Luria/Photodisc/Getty Images
Wat is fenolftaleïne?
Fenolftaleïne (C20 H14 O4 ) is een zwak zure, witte tot gele kristallijne vaste stof. Het lost gemakkelijk op in alcoholen en is enigszins oplosbaar in water. Dit organische molecuul is de hoeksteen van veel zuur-base-testen in scheikundige laboratoria.
Hoe ionisatie de kleurverandering stimuleert
In oplossing bestaat fenolftaleïne in evenwicht tussen een kleurloze geprotoneerde vorm en een roze gedeprotoneerd ion. Wanneer een oplossing zuur is, verschuiven waterstofionen het evenwicht naar de kleurloze vorm, waardoor de indicator transparant wordt. In basische media bevorderen hydroxide-ionen de vorming van het roze ion, waardoor de oplossing zijn karakteristieke tint krijgt. Deze verschuiving is een direct gevolg van de delokalisatie van elektronen die optreedt bij ionisatie.
Moleculaire structuur in zure versus alkalische omgevingen
De geprotoneerde (zure) en gedeprotoneerde (alkalische) vormen verschillen structureel. Het gedeprotoneerde ion beschikt over een uitgebreid π-elektronensysteem dat zichtbaar licht absorbeert rond 553 nm (groene gebied), dat door het menselijk oog als roze wordt waargenomen. Hoe alkalischer de oplossing, hoe groter de ionisatiegraad en hoe dieper de roze kleur.
pH-bereik van fenolftaleïne
De pH-schaal varieert van 0 tot 14, waarbij 7 als neutraal staat. Fenolftaleïne blijft kleurloos onder pH 8,2. Het begint vaag roze te worden bij een pH van 8,2 en wordt intenser tot helder magenta bij een pH van 10 en hoger, waardoor het een ideale indicator is voor zwak basische oplossingen.
Geschiedenis, productie en praktisch gebruik
Fenolftaleïne, ontdekt in 1871 door de Duitse chemicus Adolf von Baeyer, wordt geproduceerd door fenol te laten samensmelten met ftaalzuuranhydride in aanwezigheid van zwavelzuur of zinkchloride – processen die vandaag de dag nog steeds standaard zijn. In het laboratorium wordt het voornamelijk gebruikt bij zuur-base-titraties:een bekende baseconcentratie wordt getitreerd tegen een onbekende zure oplossing, en het moment dat de kleur verandert van kleurloos naar roze, duidt het equivalentiepunt aan. Historisch gezien diende fenolftaleïne als laxeermiddel in vrij verkrijgbare preparaten zoals Ex-Lax, maar het werd in 1999 in de Verenigde Staten verboden nadat studies het in verband brachten met het risico op kanker.
Hoofdlijnen
- North Node Retrograde:ontgrendel uw spirituele doel en groei
- Onderzoekers verkrijgen gegevens over de ontwikkeling van kippenembryo's
- Wat betekent forsts in de wetenschap?
- Hoe is de constructie van een biologische sleutel anders dan classificatie?
- Differentiatie van plantencellen:inzicht in gespecialiseerde structuren en functies
- Wat is gemaakt van cellen kurk spons houten plastic of boom?
- Wat zijn vier voorbeelden van imperfecte schimmel?
- Hoe kon je zien dat de bacteriën in kweek groeiden?
- Wat is de naam van enzym geproduceerd in speekselklieren?
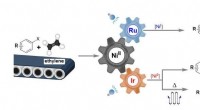
- Katalytische transformatie van ethyleen
- Blauw versus rood lakmoespapier:hoe ze zuren en basen onthullen

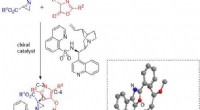
- Asymmetrische synthese van aziridine met een nieuwe katalysator kan helpen bij de ontwikkeling van nieuwe medicijnen
- Waarom bewaarde lijnolie bitter smaakt en hoe dit te corrigeren

- Miniatuur sanitair versnelt de ontwikkeling van medicijnen

 Kan de kwantumtheorie verklaren waarom grappen grappig zijn?
Kan de kwantumtheorie verklaren waarom grappen grappig zijn? Wilt u weten wat klimaatverandering in uw achtertuin doet? Daar is een dataset voor
Wilt u weten wat klimaatverandering in uw achtertuin doet? Daar is een dataset voor NaCl begrijpen:ionische binding en elektronenoverdracht
NaCl begrijpen:ionische binding en elektronenoverdracht  Is steenkool een extrusieve stollingsgesteente?
Is steenkool een extrusieve stollingsgesteente?  Kunnen we de kernwapens van de wereld volgen?
Kunnen we de kernwapens van de wereld volgen?  Uit onderzoek blijkt waarom sommige bedrijven door activisten worden 'benoemd en beschaamd'
Uit onderzoek blijkt waarom sommige bedrijven door activisten worden 'benoemd en beschaamd'  Waar wordt Earth Gravitationl Force nul?
Waar wordt Earth Gravitationl Force nul?  Welke soorten uitbarstingen heeft de vulkaan Surtsey?
Welke soorten uitbarstingen heeft de vulkaan Surtsey?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


