
Wetenschap
ΔH berekenen:een praktische gids voor enthalpieveranderingen
Door Ari Reid Bijgewerkt op 30 augustus 2022
tverkhovinets/iStock/Getty Images
Bij een chemische reactie ΔH vertegenwoordigt de enthalpieverandering en wordt berekend als de som van de standaard vormingswarmte (ΔH°f) van de producten minus de som van die van de reactanten. De eenheid is kilojoules per mol (kJ/mol).
Enthalpie (H) is een thermodynamische eigenschap die gelijk is aan de interne energie van het systeem plus het product van de druk en het volume ervan (H =U + PV). Het symbool Δ geeft een verandering aan, dus ΔH is het verschil in enthalpie tussen producten en reactanten onder dezelfde omstandigheden.
Om ΔH te bepalen heb je een uitgebalanceerde chemische vergelijking nodig, nauwkeurige ΔH°f-waarden en de aanname dat de reactie plaatsvindt bij constante druk.
Stap 1
Breng de vergelijking zo in evenwicht dat het aantal atomen van elk element aan beide kanten identiek is. De reactie tussen water en koolstof om koolmonoxide en waterstofgas te vormen wordt bijvoorbeeld geschreven als:
H₂O + C → CO + H₂
Stap 2
Zoek de standaardformatiewarmte op voor elke soort in de reactie. Betrouwbare bronnen zijn onder meer de meeste scheikundeboeken, peer-reviewed databases of het NIST Chemistry WebBook. Voor het voorbeeld:
- ΔH°f (H₂O, vloeistof) =–285,83 kJ/mol
- ΔH°f (CO, gas) =–110,53 kJ/mol
- ΔH°f (H₂, gas) =0 kJ/mol
- ΔH°f (C, vast) =0 kJ/mol
Wanneer een soort meerdere keren voorkomt in de evenwichtige vergelijking, vermenigvuldig dan de ΔH°f met de stoichiometrische coëfficiënt.
Stap 3
Bereken de totale ΔH°f voor de reactanten:
(–285,83 kJ/mol) + (0 kJ/mol) =–285,83 kJ/mol
Stap 4
Bereken de totale ΔH°f voor de producten:
(–110,53 kJ/mol) + (0 kJ/mol) =–110,53 kJ/mol
Stap 5
Bepaal ΔH door de som van de reactanten af te trekken van de productsom:
ΔH =–110,53 kJ/mol – (–285,83 kJ/mol) =+175,3 kJ/mol
Een positieve ΔH duidt op een endotherm proces, wat betekent dat de reactie warmte uit de omgeving absorbeert.
 De voordelen van bitter zijn:hoe de evolutie van de cranberry er een Thanksgiving-hoofdbestanddeel van maakte
De voordelen van bitter zijn:hoe de evolutie van de cranberry er een Thanksgiving-hoofdbestanddeel van maakte  Hele hellingen van bomen werden deze zomer bruin. Is dit het begin van de ineenstorting van het ecosysteem?
Hele hellingen van bomen werden deze zomer bruin. Is dit het begin van de ineenstorting van het ecosysteem? Wat is Natural Lube?
Wat is Natural Lube?  Niets om over te niezen:experimenteel model toont aan dat stuifmeel het weer kan veranderen
Niets om over te niezen:experimenteel model toont aan dat stuifmeel het weer kan veranderen  In een gebied naast een rivier zijn er veel bomen. Deze weinig erosie vindt plaats. het beste uitlegt dit?
In een gebied naast een rivier zijn er veel bomen. Deze weinig erosie vindt plaats. het beste uitlegt dit?
Hoofdlijnen
- Waterweed groeit in de buurt van het wateroppervlak in meren en vijvers. Het is vaak dichte klonten. is waargenomen dat chloroplasten deze plant in de cel bewegen. Hoe kan B?
- Wat is Brevundimonas vesicularis?
- Hoe werken onze spieren? Wetenschappers onthullen belangrijke nieuwe inzichten in spiereiwitten
- Drie soorten dieren die filtervoeding gebruiken om aan voedsel te komen?
- Is fytoplankton een type plant?
- Welke fysieke kenmerken is waarschijnlijk een gevolg van erfenis?
- Wat onderscheidt levende organismen van niet-levende materie?
- Hoeveel cellen zijn er allemaal in een menselijk lichaam samen?
- Wat is de basisdefinitie van een prokaryotische cel?
- Eenden bieden onderzoekers een unieke kans om menselijke aanraking te bestuderen
- Katalysatoren voor een betere productie van biobrandstoffen

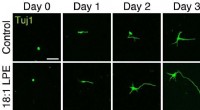
- Oleoyl-LPE oefent neurietstimulatie en neuroprotectie uit
- Hoogrenderende katalysator verbetert de elektrische reductieprestaties van kooldioxide

- De algehele reactievolgorde begrijpen:hoe concentratie de reactiesnelheid beïnvloedt

 Kunnen twee NASA-astronauten tot volgend jaar vastzitten in het ruimtestation? Dit is wat u moet weten
Kunnen twee NASA-astronauten tot volgend jaar vastzitten in het ruimtestation? Dit is wat u moet weten  Bevriezen in record dieptepunten? Je twijfelt misschien aan de opwarming van de aarde, zegt wetenschapper
Bevriezen in record dieptepunten? Je twijfelt misschien aan de opwarming van de aarde, zegt wetenschapper Goud zeven uit de datastroom
Goud zeven uit de datastroom Is de vruchtbare halve maan in Europa of Noord-Amerika?
Is de vruchtbare halve maan in Europa of Noord-Amerika?  Hoe knaagdieren te identificeren aan de hand van hun uitwerpselen
Hoe knaagdieren te identificeren aan de hand van hun uitwerpselen Wat zijn de reacties van TFA?
Wat zijn de reacties van TFA?  Een nieuwe tool voor het beheersen van reacties in microrobots en microreactoren
Een nieuwe tool voor het beheersen van reacties in microrobots en microreactoren Wat is de meest zuidelijke staat in het noordoosten?
Wat is de meest zuidelijke staat in het noordoosten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

