
Wetenschap
Het berekenen van subatomaire deeltjes in atomen:een praktische gids
Door Andrew Youngker Bijgewerkt op 30 augustus 2022
Emilija Randjelovic/iStock/GettyImages
Subatomaire deeltjes zijn de individuele protonen, neutronen en elektronen waaruit de samenstelling van atomen bestaat. Met behulp van het periodiek systeem der elementen kunnen we berekenen hoeveel subatomaire deeltjes er in een bepaald atoom zitten. Protonen en neutronen worden gevonden in de kern van een atoom, terwijl elektronen de kern omringen. De atoommassa of het massagetal wordt meestal als decimaal gegeven, vanwege het aantal gevonden isotopen en hun relatieve overvloed. Sommige bekende isotopen hebben een specifiek aantal neutronen en zijn nuttig als het over radioactieve materialen gaat.
Basis subatomaire berekeningen
Stap 1
Zoek het atoomnummer van een bepaald element in het periodiek systeem; dit is het aantal protonen dat in de kern wordt aangetroffen. Het wordt meestal boven het elementsymbool vermeld. De identiteit van een element is gebaseerd op het aantal protonen dat zich in de kern bevindt.
Stap 2
Bepaal het aantal elektronen met behulp van het atoomnummer. Een atoom heeft een neutrale lading, dus de positieve en negatieve lading zijn aan elkaar gelijk. Het atoomnummer is tevens het aantal elektronen.
Stap 3
Bereken het aantal neutronen door het massagetal te nemen en het aantal protonen in de kern af te trekken. Het massagetal bevindt zich meestal onder het elementsymbool en geeft aan hoeveel een element zou wegen in grammen gegeven een mol van de stof. Omdat de massa gecentraliseerd is in de kern, dragen alleen de protonen en neutronen bij aan het massagetal.
Isotope Calculations
Stap 1
Zoek het atoomnummer voor het aantal protonen en elektronen in het atoom in het periodiek systeem. Het aantal protonen en elektronen is gelijk aan het atoomnummer.
Stap 2
Bereken het aantal neutronen door het atoomnummer af te trekken van het isotoopnummer. Koolstof 14 heeft bijvoorbeeld een isotoopmassa van 14 en 6 protonen, dus het aantal neutronen is gelijk aan 8.
Stap 3
Isotopen zijn elementen die qua massa verschillen. Omdat massa wordt afgeleid van de kern en protonen de identiteit van een element geven, verschilt het aantal neutronen in isotopen.
Dingen die nodig zijn
- Rekenmachine
- Periodiek systeem der elementen
TL;DR (te lang; niet gelezen)
Atomen zijn elektrisch neutraal; de positieve en negatieve ladingen zijn gelijk.
 Wat is Living Rock?
Wat is Living Rock?  Onderzoeker ontdekt hoe stereotypen over genialiteit de beslissing van vrouwen bepalen om psychologie of filosofie te gaan studeren
Onderzoeker ontdekt hoe stereotypen over genialiteit de beslissing van vrouwen bepalen om psychologie of filosofie te gaan studeren  Duurzame landbouw:opbrengst garanderen en broeikasgassen verminderen
Duurzame landbouw:opbrengst garanderen en broeikasgassen verminderen De manier waarop levende materie verschilt van niet -is?
De manier waarop levende materie verschilt van niet -is?  Sterkte van de wereldwijde stratosferische circulatie voor het eerst gemeten
Sterkte van de wereldwijde stratosferische circulatie voor het eerst gemeten
Hoofdlijnen
- Geavanceerde microscopen helpen wetenschappers begrijpen hoe cellen eiwitten afbreken
- Kan glucose door het celmembraan diffunderen door eenvoudige diffusie?
- Waar is het grootste deel van de activiteit gericht tijdens de G2 -fasecelcyclus?
- Waar gebruiken cellen voor verteerd voedsel voor?
- Wat dient als het controlecentrum voor een celmetabolisme en reproductie?
- Welk orgaan produceert lipase?
- Welk instrument meet het gewicht van een worm?
- Cellen bevatten onderdelen die bekend staan als organellen. Deze zijn gespecialiseerd. Wat betekent dit?
- Wat zijn de basisparen bij het repliceren van DNA?
- Ruwe oppervlakken bieden extra locaties voor energieopwekkende reacties in brandstofcellen
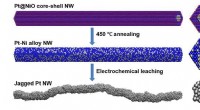
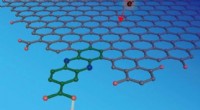
- Experimenten en analyses laten zien hoe elektronen en protonen samenkomen op een elektrodeoppervlak
- De lengte van een gebogen lijn (boog) berekenen - een praktische gids

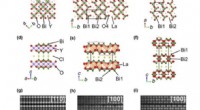
- Bronnen voor teambeeldvorming die worden gebruikt in internationale experimenten met nieuwe fotokatalysatoren
- Nieuwe gel verhoogt celoverleving in beschadigd hersenweefsel
 Vind je de normale vries- en kookpunten van 21,2 g NaCl in 135 ml water?
Vind je de normale vries- en kookpunten van 21,2 g NaCl in 135 ml water?  Renault riskeert een slechte kredietwaardigheid, S&P waarschuwt
Renault riskeert een slechte kredietwaardigheid, S&P waarschuwt Waarom staat de wetenschap open voor verandering?
Waarom staat de wetenschap open voor verandering?  Nieuw onderzoek onderzoekt hoe multinationale bedrijven corruptie kunnen beheersen
Nieuw onderzoek onderzoekt hoe multinationale bedrijven corruptie kunnen beheersen  Wat is de afstand tussen kernen van verschillende bindingen?
Wat is de afstand tussen kernen van verschillende bindingen?  Wat is de enige vloeistof in groep 17 van periodieke grafiek?
Wat is de enige vloeistof in groep 17 van periodieke grafiek?  Wanneer chloor reageert met een metalen element om een ionische verbinding te maken, vormt het wat?
Wanneer chloor reageert met een metalen element om een ionische verbinding te maken, vormt het wat?  Om recycling te stimuleren, beloon consumenten met kortingen, deals en sociale connecties
Om recycling te stimuleren, beloon consumenten met kortingen, deals en sociale connecties
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

