
Wetenschap
Waarom enzymen falen:door hitte geïnduceerde denaturatie en chemische remming
Creatas/Creatas/Getty Images
Enzymen zijn gespecialiseerde eiwitten die biochemische reacties katalyseren door nauwkeurige driedimensionale structuren aan te nemen. Wanneer hun vorm wordt verstoord, verliezen ze hun activiteit. Twee primaire mechanismen verminderen de effectiviteit van enzymen:door hitte geïnduceerde denaturatie en chemische remming.
Denaturatie door hitte
In een stabiel enzym trillen de atomen, maar blijft de eiwitketen gevouwen. Het verhogen van de temperatuur verhoogt de moleculaire beweging, waardoor het enzym zich uiteindelijk ontvouwt en zijn functionele conformatie verliest. De meeste dierlijke enzymen bereiken hun piekactiviteit rond de fysiologische temperatuur (≈37°C) en beginnen hun activiteit te verliezen zodra de temperatuur ongeveer 40°C overschrijdt. Extremofiele bacteriën beschikken echter over enzymen die bestand zijn tegen temperaturen rond het kookpunt, waardoor ze kunnen gedijen in warmwaterbronnen.
Actieve site:de reactiehub
De actieve plaats is de katalytische pocket van het enzym, analoog aan een mond die het substraat vasthoudt. Een juiste uitlijning van specifieke zijketens van aminozuren is essentieel voor het binden van het substraat en het vergemakkelijken van de chemische transformatie. Als de 3D-vorm van de actieve plaats vervormd is, kan het enzym zijn reactie niet uitvoeren.
Concurrentieremmers
Competitieve remmers bootsen het substraat na en binden zich rechtstreeks aan de actieve plaats, waardoor de toegang tot het substraat wordt geblokkeerd. Omdat ze kunnen dissociëren, zijn veel daarvan omkeerbaar en zorgen ervoor dat het enzym weer actief wordt zodra de remmer is verwijderd.
Niet-competitieve (allosterische) remmers
Deze remmers hechten zich aan andere regulerende plaatsen dan de actieve plaats. Binding verandert de conformatie van het enzym, waardoor de actieve site effectief wordt gesloten of uitgeschakeld. Allosterische remming kan tegelijkertijd hele enzymcomplexen tot zwijgen brengen wanneer een enkele remmer zich bindt aan de regulerende regio van één subeenheid.
Het begrijpen van deze mechanismen is van cruciaal belang voor gebieden variërend van het ontwerpen van geneesmiddelen tot industriële biotechnologie.
 Wat is een chemische stof die de groei van planten beïnvloedt?
Wat is een chemische stof die de groei van planten beïnvloedt?  Mieren geven hun giftige geheimen prijs
Mieren geven hun giftige geheimen prijs Wat zijn de kleine kralen in handdesinfecterend middel? Hun doel en impact begrijpen
Wat zijn de kleine kralen in handdesinfecterend middel? Hun doel en impact begrijpen  Wat is het proces dat water van gasvormige vorm naar een vloeibare vorm brengt?
Wat is het proces dat water van gasvormige vorm naar een vloeibare vorm brengt?  Biologisch afbreekbare verpakking ontwikkeld voor biologische schoonheidsmarkt
Biologisch afbreekbare verpakking ontwikkeld voor biologische schoonheidsmarkt
 Principes van pneumatische systemen
Principes van pneumatische systemen Wat zijn de takken van een vallend blad volgens de natuurkunde?
Wat zijn de takken van een vallend blad volgens de natuurkunde?  NASA vindt een oog en een gigantische staart in tyfoon Hagupit
NASA vindt een oog en een gigantische staart in tyfoon Hagupit Boomringen van oude Douglas-sparren aan de kust van Oregon tonen bewijs van 1700 tsunami
Boomringen van oude Douglas-sparren aan de kust van Oregon tonen bewijs van 1700 tsunami 100 miljoen dode bomen in de Sierra vormen een enorm risico voor onvoorspelbare bosbranden
100 miljoen dode bomen in de Sierra vormen een enorm risico voor onvoorspelbare bosbranden
Hoofdlijnen
- Zonder te ruimen, Victoria's plan voor wilde paarden lijkt te mislukken
- Wat transporteert vaste deeltjes in een cel?
- Waar in de cel wordt DNA gekopieerd?
- Welke plantencelorganel vangt en slaat zonlichtergie op voor fotosynthese?
- Welk type zaad zit er in de rode bonen?
- Onderzoek toont aan waardoor de celwanden van planten worden samengedrukt en uitgerekt
- Ontcijferen hoe virussen ervoor kiezen om al dan niet hun bacteriële gastheer te worden
- Hoe werken de verschillende soorten cellen om longen schoon te maken?
- Welke informatie bieden genen?
- Een afstembaar 2D covalent netwerk voor ladingsselectieve verwijdering van giftige kleurstoffen uit afvalwater

- Psoriasis voorkomen met vanilline
- De kunst van het balanceren van chemische vergelijkingen beheersen:een praktische gids
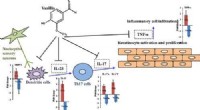
- Genetische oorzaak van ALS en frontotemporale dementie geblokkeerd door RNA-bindende verbinding

- Een beter duurzaam maandverband

 Wanneer de erfenis van een bepaalde eigenschap volgt Patroon Wat?
Wanneer de erfenis van een bepaalde eigenschap volgt Patroon Wat?  Wat is een voorbeeld van een in water oplosbare vitamine?
Wat is een voorbeeld van een in water oplosbare vitamine?  Hoe vormen aurora's zich in de ionosfeer?
Hoe vormen aurora's zich in de ionosfeer?  Wanneer liet Sir Isaac Newton de metalen ballen vallen van leunende toren van Pisa?
Wanneer liet Sir Isaac Newton de metalen ballen vallen van leunende toren van Pisa?  Nieuwe chemie vinden om het dubbele van de koolstof vast te leggen
Nieuwe chemie vinden om het dubbele van de koolstof vast te leggen  Royale voordelen staan gelijk aan gelukkige werknemers? Niet altijd. Dit is wat werknemers echt willen
Royale voordelen staan gelijk aan gelukkige werknemers? Niet altijd. Dit is wat werknemers echt willen  3D-printer maakt vredesmissies goedkoper en reparatie van verdedigingssystemen sneller
3D-printer maakt vredesmissies goedkoper en reparatie van verdedigingssystemen sneller Het homeostatische mechanisme bij mensen dat de pH van de bloedreguleert, hangt af van de feedback van informatie uit?
Het homeostatische mechanisme bij mensen dat de pH van de bloedreguleert, hangt af van de feedback van informatie uit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

