
Wetenschap
Wat blijft er behouden bij chemische reacties? De wet van behoud van materie begrijpen
Door David Dunning, bijgewerkt op 30 augustus 2022
Behoud van materie
Het fundamentele principe van de chemie, de Wet van Behoud van Materie, stelt dat materie niet kan worden gecreëerd of vernietigd in een gesloten systeem. Bij een typische chemische reactie is de totale massa van de reactanten gelijk aan de totale massa van de producten. Dit betekent dat de hoeveelheid materie voor en na de reactie constant blijft.
Illustratief voorbeeld:vorming van water
Beschouw de reactie van waterstofgas (H₂) met zuurstofgas (O₂) om water (H₂O) te vormen. Eén mol water bevat twee mol waterstof en één mol zuurstof. In termen van massa reageert 2,02 g waterstof met 16 g zuurstof om 18,02 g water te produceren, wat perfect het behoud van massa illustreert.
Empirische formules bepalen
De wet staat scheikundigen ook toe de empirische formule van een onbekende verbinding af te leiden. Door de massa van elk element in een monster te meten en de resulterende verhoudingen terug te brengen tot hun eenvoudigste gehele getalvorm, kan de empirische formule worden bepaald.
Atoomeconomie en groene chemie
Atoomeconomie verwijst naar de fractie van reactantatomen die in het gewenste product terechtkomen. Reacties met een hoge atoomeconomie zetten het grootste deel van het uitgangsmateriaal om in bruikbare producten, waardoor minder afval ontstaat. Dergelijke processen staan centraal in groene chemie-initiatieven die gericht zijn op het verminderen van de impact op het milieu.
Het begrijpen van deze principes is essentieel voor scheikundigen, ingenieurs en iedereen die met chemische processen werkt.
 Wat is methanolontleding?
Wat is methanolontleding?  Hoeveel milliliter van een 100,00 m oplossing zoutzuur is nodig om volledig te reageren met 45,5 g zinksulfide volgens de hieronder getoonde chemische reactie?
Hoeveel milliliter van een 100,00 m oplossing zoutzuur is nodig om volledig te reageren met 45,5 g zinksulfide volgens de hieronder getoonde chemische reactie?  Optimalisatie van de elektrolyten van lithium-zwavelbatterijen voor een lange levensduur
Optimalisatie van de elektrolyten van lithium-zwavelbatterijen voor een lange levensduur Covalente obligaties:het delen van elektronen en de octetregel begrijpen
Covalente obligaties:het delen van elektronen en de octetregel begrijpen  Effectieve manieren om totaal opgeloste vaste stoffen (TDS) uit drinkwater te verwijderen
Effectieve manieren om totaal opgeloste vaste stoffen (TDS) uit drinkwater te verwijderen
 Na de aardbeving tussen Iran en Irak, seismologen werken aan het invullen van de foutenkaart van de regio
Na de aardbeving tussen Iran en Irak, seismologen werken aan het invullen van de foutenkaart van de regio Welke eigenschappen moet een object bezitten om het concept van mineralen te conformeren?
Welke eigenschappen moet een object bezitten om het concept van mineralen te conformeren?  Wetenschappers meten nieuwe diepten aan de onderkant van de hydrologische cyclus
Wetenschappers meten nieuwe diepten aan de onderkant van de hydrologische cyclus Waarom is pollen geel?
Waarom is pollen geel?  Hoe kunnen steden gezonder worden, groener, en rechtvaardiger in de toekomst?
Hoe kunnen steden gezonder worden, groener, en rechtvaardiger in de toekomst?
Hoofdlijnen
- Wat is het oorspronkelijke doel voor het classificeren van organismen?
- Welk deel van de cel bevat erfelijke informatie?
- Welke cellen hebben gericht?
- Welke organellen zijn betrokken bij eiwitsynthese de cel?
- Welk kenmerk wordt genoemd als het celmembraan alleen bepaalde moleculen en ionen de cel binnenlaat of verlaat?
- Hoe de evolutie de optimale botstructuur bij springende knaagdieren voorbijschoot
- Welke techniek zou een wetenschapper gebruiken om specifieke organel te isoleren?
- Doe-het-zelf-virussen:hoe virussen zichzelf assembleren
- De epidermis is verantwoordelijk voor het beschermen van het lichaam tegen invasie van bacteriën en andere buitenlandse middelen, vooral omdat het bestaat uit?
- Huidig model voor opslag kernafval is onvolledig

- Nieuw bewijsmateriaal ingediend bij Grenfell Tower Inquiry over bekledingsreactiviteit

- Neutronen onthullen snelle translatie van methaan op het grensvlak van twee clathraatstructuren
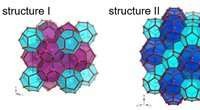
- Zelfassemblage in meerdere stappen opent de deur naar nieuwe herconfigureerbare materialen

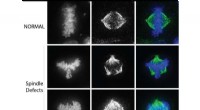
- Een nieuw mechanisme in celdeling ontdekken
 Is Germanium een dirigent of een isolator?
Is Germanium een dirigent of een isolator?  Hoe zijn de elektronen rond nucleus gerangschikt en hoe zij de reactiviteit beïnvloeden?
Hoe zijn de elektronen rond nucleus gerangschikt en hoe zij de reactiviteit beïnvloeden?  Indringte stollingsgesteente wordt gekoeld en gestold boven de grond?
Indringte stollingsgesteente wordt gekoeld en gestold boven de grond?  Als de beweging van 1 deeltje een gas niet wordt beïnvloed door andere deeltjes, tenzij wat?
Als de beweging van 1 deeltje een gas niet wordt beïnvloed door andere deeltjes, tenzij wat?  3 Waarom is het belangrijk dat er tijdens de destillatie een stroom koel water rond de condensor stroomt?
3 Waarom is het belangrijk dat er tijdens de destillatie een stroom koel water rond de condensor stroomt?  Eencellige organismen kunnen niet reageren op hun omgeving?
Eencellige organismen kunnen niet reageren op hun omgeving?  Snel, eenvoudige nieuwe beoordeling van aardbevingsgevaar
Snel, eenvoudige nieuwe beoordeling van aardbevingsgevaar Wat gebeurt er als u een object voor een licht plaatst?
Wat gebeurt er als u een object voor een licht plaatst?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

