
Wetenschap
Mollen beheersen in de chemie:een praktische gids voor molaire massa en stoichiometrie
Door Judy Tyler | Bijgewerkt op 30 augustus 2022
In de scheikunde is dit een mol is de fundamentele eenheid die het aantal deeltjes aan de massa koppelt in stoichiometrische vergelijkingen. Eén mol van welke stof dan ook bevat precies 6,02×10²³ atomen, ionen of moleculen, een waarde die bekend staat als het getal van Avogadro. De massa van één mol, de molaire massa genoemd —is numeriek gelijk aan het massagetal van het element in grammen. Voor verbindingen is de molaire massa de som van de atoommassa's van alle samenstellende atomen in de juiste verhoudingen.
De molaire massa van een element bepalen
Stap 1 – Identificeer het element
Zoek lithium (Li) op het periodiek systeem. Het atoomnummer, 3, geeft het aantal protonen in elke kern aan.
Stap 2 – Noteer het massanummer
Het massagetal van lithium is 6,94, het gecombineerde aantal protonen en neutronen in de kern.
Stap 3 – Bereken de molmassa
Omdat het massagetal gelijk is aan de massa in grammen van één mol, is de molaire massa van lithium 6,94gmol⁻¹ .
Het bepalen van de molecuulmassa van een chemische verbinding
Stap 1 – Selecteer de verbinding
Kies koolstofdioxide (CO₂) als voorbeeld. Identificeer de samenstellende atomen (koolstof en zuurstof) in het periodiek systeem.
Stap 2 – Atoommassa's ophalen
Koolstof heeft een atoommassa van 12,01 gmol⁻¹ en die van zuurstof is 16,00 gmol⁻¹.
Stap 3 – Tel de bijdragen op
De molecuulmassa van CO₂ wordt berekend als 12,01+2(16,00)=44,01gmol⁻¹ .
Omzetten van massa naar mol
Stap 1 – Identificeer de substantie en massa
Bepaal hoeveel mol er aanwezig is in 600 g water (H₂O) . Houd er rekening mee dat de molaire massa van water 18,02 gmol⁻¹ is.
Stap 2 – Stel de proportionele relatie in
xmolH₂O=(1molH₂O/18,02gH₂O)×600gH₂O
Stap 3 – Bepaal het aantal mol
Het oplossen van de vergelijking levert ≈33,3mol op water in 600 g vloeistof.
Deze eenvoudige berekeningen vormen de basis voor nauwkeurige stoichiometrische analyses en kwantitatief chemisch onderzoek.
 Wanneer metalen lithium wordt gesneden, is het fysische of chemische verandering?
Wanneer metalen lithium wordt gesneden, is het fysische of chemische verandering?  Hoe ijsdeeltjes de vorming van radicalen bevorderen
Hoe ijsdeeltjes de vorming van radicalen bevorderen  Hoeveel protonen neutronen en elektronen zijn er in een neutraal atoom van 113 inin
Hoeveel protonen neutronen en elektronen zijn er in een neutraal atoom van 113 inin  Plastics van de toekomst zullen vele vorige levens leiden, dankzij chemische recycling
Plastics van de toekomst zullen vele vorige levens leiden, dankzij chemische recycling Hoe zou je goudstof scheiden van een mengsel van ijzervijlsel en zout?
Hoe zou je goudstof scheiden van een mengsel van ijzervijlsel en zout?
 Palmolie:Minder kunstmest en geen herbicide maar dezelfde opbrengst?
Palmolie:Minder kunstmest en geen herbicide maar dezelfde opbrengst? Wat eten Zee Sint-jakobsschelpen en waar wonen ze?
Wat eten Zee Sint-jakobsschelpen en waar wonen ze?  Klimaatverandering leidt tot ingrijpende, onmiddellijke en verergerende gevolgen voor de gezondheid, meer dan 120 onderzoekers zeggen:
Klimaatverandering leidt tot ingrijpende, onmiddellijke en verergerende gevolgen voor de gezondheid, meer dan 120 onderzoekers zeggen: Sociaal-economisch, milieueffecten van COVID-19 gekwantificeerd
Sociaal-economisch, milieueffecten van COVID-19 gekwantificeerd Welk insect eet motten?
Welk insect eet motten?
Hoofdlijnen
- Wat maakt fysieke kenmerken een onvoldoende basis voor het groeperen van leden van een soort?
- Welke organismen die niet hun eigen voedsel kunnen maken, zijn?
- Welke wetenschapper gaf de naamcellen aan structuren die hij zag?
- Welke twee categorieën worden gebruikt om deeltjes te classificeren?
- Sociale vaardigheden van honden gekoppeld aan gevoeligheid voor oxytocine
- Wat kunnen zakpijpen ons vertellen over neurodegeneratie?
- Hoe worden groepen genoemd?
- Waarom hebben we grote hersenen?
- Leden van een soort zijn nauw verwant en kunnen paren om welke nakomelingen te produceren?
- Zelfvouwende origami:Dankzij chemische programmering kunnen Nafion-vellen worden gevouwen en opnieuw gevouwen

- Video:Waarom werkt onkruidverdelger niet meer?

- Onderzoek wijst op een sterke impact van waterzuivering tot medicijnproductie

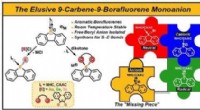
- Stabilisatie van het borafluoreen-anion met carbenen
- Van insect tot medicijn - speeksel van teken kan de sleutel zijn tot de behandeling van hartaandoeningen

 Waar bevindt de constellatie Taurus zich in de lucht?
Waar bevindt de constellatie Taurus zich in de lucht?  We kunnen onze vis eten en ook klimaatverandering bestrijden
We kunnen onze vis eten en ook klimaatverandering bestrijden In kaart brengen en meten van eiwitten op de oppervlakken van endoplasmatisch reticulum (ER) in cellen
In kaart brengen en meten van eiwitten op de oppervlakken van endoplasmatisch reticulum (ER) in cellen Wat is de pH wanneer hydraniumconcentratie H3O 1,47?
Wat is de pH wanneer hydraniumconcentratie H3O 1,47?  Hoe kun je zien of een zuur is geneutraliseerd?
Hoe kun je zien of een zuur is geneutraliseerd?  Wat is in een cel de energie die in voedsel is opgeslagen, gerust?
Wat is in een cel de energie die in voedsel is opgeslagen, gerust?  Wat is een andere naam voor een suikerplant?
Wat is een andere naam voor een suikerplant?  Wat is de uitgebalanceerde vergelijking voor kobalt III-nitraat en lithiumhydroxide?
Wat is de uitgebalanceerde vergelijking voor kobalt III-nitraat en lithiumhydroxide?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

