
Wetenschap
Protonen versus elektronen:hoe ze de bouwstenen van materie vormen
Door Lesley Barker – Bijgewerkt op 30 augustus 2022
Overzicht van de atomaire structuur
Atomen zijn de fundamentele eenheden van materie, elk op unieke wijze gedefinieerd door hun elektronen-, proton- en neutronenconfiguratie. Deze structuur bepaalt de identiteit van een element.
Elektronen:de negatieve wolk
Elektronen zijn vrijwel massaloze, negatief geladen deeltjes die in discrete energieschillen rond de kern cirkelen. De maximale bezetting van elke schil volgt de 2n²-regel, en de ruimtelijke verdeling wordt vaak beschreven als een elektronenwolk of golffunctie.
Protonen:positieve kern
Protonen, die zich in de kern bevinden, hebben een positieve lading die in grootte gelijk is aan die van een elektron. Hun aantrekkingskracht op elektronen handhaaft de ladingsneutraliteit in neutrale atomen. Het aantal protonen (het atoomnummer) identificeert een element op unieke wijze.
Neutronen:kernlijm
Neutronen, die zich ook in de kern bevinden, hebben geen netto lading, maar zorgen voor de sterke kernkracht die protonen aan elkaar bindt. Zoals Anthony Carpi van de City University of New York uitlegt, werken neutronen als ‘lijm’, waardoor wordt voorkomen dat de afstotende krachten tussen positief geladen protonen de kern destabiliseren.
Laadbalans en ionen
In een neutraal atoom zijn de aantallen protonen en elektronen identiek. Wanneer dit evenwicht wordt verstoord, worden de resulterende geladen soorten ionen genoemd, geen atomen.
Atoomnummers en massa
Het atoomnummer (Z) telt protonen en, in een neutraal atoom, ook elektronen. Het atoomgewicht (of massagetal) benadert de som van protonen en neutronen en is te vinden in het Periodiek Systeem der Elementen.
Deskundig inzicht
Zowel elektronen als protonen zijn geladen subatomaire deeltjes; hun ladingstekens verschillen, en elektronen zijn feitelijk gewichtloos, terwijl protonen een meetbare massa hebben. Elektronen draaien rond de kern en worden aangetrokken door de positieve lading van de protonen.
Historische mijlpalen:J.J. Thomson ontving in 1906 de Nobelprijs voor de ontdekking van het elektron, en Ernest Rutherford identificeerde het proton in 1918.
Voor meer informatie, zie het Periodiek Systeem der Elementen .
Hoofdlijnen
- Hoe wordt het voedsel geleidend weefsel van een plant genoemd?
- Wat biedt ATP?
- Welke structuur zou een eencellig organisme waarschijnlijk moeten bewegen?
- Wat is een complex koolhyraat dat plantenstelen en wortels versterkt?
- Eubacteria en Archaea:de twee prokaryotische koninkrijken uitgelegd
- Wat is selectie in de wetenschap?
- Wat is het proces van welke organismen nakomelingen produceren om hun soort te bestendigen?
- Wie heeft de term cel geïntroduceerd?
- Welke klier laat zijn secretie in de bloedbaan vrij?
- Belangrijkste mechanismen van luchtwegontspanning bij astma onthuld in nieuwe studie
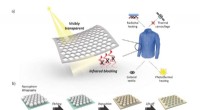
- Nieuwe nanofotonische coating kan bijdragen aan thermisch beheer en contra-surveillance
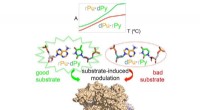
- Onderzoekers identificeren de bron van asymmetrie in RNA-DNA-hybriden
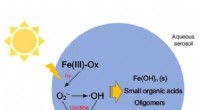
- Effecten van Fenton-achtige reacties van ijzeroxalaat op atmosferische oxidatieprocessen en stralingsforcering
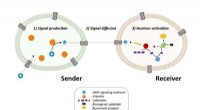
- Levensechte cellen kunnen nu over lange afstanden communiceren via signaalversterking
 Wat gebeurt er als calciumcarbonaat en zoutzuur zich vermengen?
Wat gebeurt er als calciumcarbonaat en zoutzuur zich vermengen?  Waarom neemt de oplosbaarheid van calciumchromaat af naarmate de temperatuur stijgt?
Waarom neemt de oplosbaarheid van calciumchromaat af naarmate de temperatuur stijgt?  Welke twee elektrische hoeveelheden worden gemeten in volt?
Welke twee elektrische hoeveelheden worden gemeten in volt?  Wat voor soort herten zijn in Texas?
Wat voor soort herten zijn in Texas?  Wat zijn de producten gevormd uit een reactie tussen waterstofjodide en zwavelzuur?
Wat zijn de producten gevormd uit een reactie tussen waterstofjodide en zwavelzuur?  Waar worden de carriereiwitten en kanaal gevonden?
Waar worden de carriereiwitten en kanaal gevonden?  Wat produceert de boom Boswellia Sacra?
Wat produceert de boom Boswellia Sacra?  Mars:Was Olympus Mons ooit een gigantisch vulkanisch eiland?
Mars:Was Olympus Mons ooit een gigantisch vulkanisch eiland?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


