
Wetenschap
Methanol versus isopropylalcohol:belangrijkste verschillen verklaard
Door Eri Luxton | Bijgewerkt op 30 augustus 2022
Wat is alcohol?
In het dagelijks taalgebruik verwijst ‘alcohol’ vaak naar ethanol, de drinkbare stof die in dranken zit. In de scheikunde is een alcohol echter elke verbinding die een hydroxylgroep (–OH) bevat die aan een koolstofatoom is bevestigd [1] . Als u deze definitie begrijpt, wordt duidelijk hoe methanol en isopropylalcohol van elkaar verschillen.
Methanol (CH3 OH)
Structuur:Een enkel koolstofatoom gebonden aan drie waterstofatomen en één hydroxylgroep.
Belangrijkste eigenschappen:
- Wordt vaak gebruikt als laboratoriumoplosmiddel en als bestanddeel van gedenatureerde alcohol.
- Het innemen van zelfs een kleine hoeveelheid kan leiden tot blindheid of de dood – NIH Medline rapporteert [2] .
Isopropylalcohol (C3 H7 OH)
Structuur:Een centraal koolstofatoom gebonden aan twee methylgroepen en één hydroxylgroep.
Belangrijkste eigenschappen:
- Op grote schaal gebruikt als oplosmiddel, desinfectiemiddel en reinigingsmiddel.
- Minder giftig dan methanol, maar nog steeds gevaarlijk bij inslikken; het is licht ontvlambaar.
Veiligheidswaarschuwing
Zowel methanol als isopropylalcohol zijn giftig bij inslikken, inademen of opname via de huid. Gebruik ze altijd in goed geventileerde ruimtes, draag geschikte beschermende kleding en houd ze buiten het bereik van kinderen en huisdieren.
 Wat is het type aantrekkingskracht dat twee watermoleculen bij elkaar houdt?
Wat is het type aantrekkingskracht dat twee watermoleculen bij elkaar houdt?  Welke van de volgende is een organisch molecuul ijzeroxide sucrose water of zuurstofgas?
Welke van de volgende is een organisch molecuul ijzeroxide sucrose water of zuurstofgas?  Wat gebruikt voor Berylium?
Wat gebruikt voor Berylium?  Wat is het verschil tussen gedeeltelijk molair volume en specifiek volume?
Wat is het verschil tussen gedeeltelijk molair volume en specifiek volume?  Wat zijn de kleuren van zilvermetaal en kopernitraat in water?
Wat zijn de kleuren van zilvermetaal en kopernitraat in water?
 Antarctisch Schiereiland op warmste in decennia:studie
Antarctisch Schiereiland op warmste in decennia:studie Invasieve plantensoorten nemen exponentieel toe, maar niemand weet hoeveel het er zijn
Invasieve plantensoorten nemen exponentieel toe, maar niemand weet hoeveel het er zijn  Afname van atmosferische koolstofdioxide sleutel tot oude klimaattransitie
Afname van atmosferische koolstofdioxide sleutel tot oude klimaattransitie Seismische activiteit van de alpiene breuk in Nieuw-Zeeland complexer dan vermoed
Seismische activiteit van de alpiene breuk in Nieuw-Zeeland complexer dan vermoed Convectiestromen:hoe hitte de atmosfeer, het weer en het dagelijks leven beïnvloedt
Convectiestromen:hoe hitte de atmosfeer, het weer en het dagelijks leven beïnvloedt
Hoofdlijnen
- Wat verandert specifiek in het evolutieproces?
- Tot welke klasse verbindingen behoren zetmeel en suikers?
- Wat is een voorbeeld van alchemie?
- De diversiteit van Micropsalliota blootleggen:zeven nieuwe soorten en één nieuw geregistreerde soort in Zuid-China
- Hoe kan men bepalen dat een organisme homozygoot of heterozygoot is?
- Waarom is kern aanwezig in de cel?
- Wat voor soort wetenschapper zou het organisme observeren?
- Bevat de kern genen voor overerving?
- Welke organellenfunctie is eiwitproductie voor gebruik in cel?
- Nieuw staal om de levensduur van olieveldpijpleidingen te verdubbelen

- 3D-atoomstructuur van TRPML1-ionkanaal gepubliceerd

- Rood of geel? Een eenvoudige papieren test detecteert valse of ondermaatse antibiotica

- Nieuwe stoffenbibliotheek om het zoeken naar actieve stoffen te versnellen
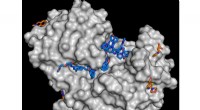
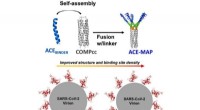
- Ontwikkeld multivalent zelf-geassembleerd bindereiwit tegen SARS-CoV-2 RBD
 De klimaatcrisis is aangebroken - dus stop met je schuldig te voelen en begin je toekomst voor te stellen
De klimaatcrisis is aangebroken - dus stop met je schuldig te voelen en begin je toekomst voor te stellen Wat zijn CH en OH -obligaties?
Wat zijn CH en OH -obligaties?  Hoe luchthavens werken
Hoe luchthavens werken  Astronomen onthullen nieuwe inzichten in de oorsprong en evolutie van open cluster NGC 6791
Astronomen onthullen nieuwe inzichten in de oorsprong en evolutie van open cluster NGC 6791 Welke eigenschappen hebben gassen die vloeistoffen niet?
Welke eigenschappen hebben gassen die vloeistoffen niet?  Plasmonische verbetering van stabiliteit en helderheid in organische lichtemitterende apparaten
Plasmonische verbetering van stabiliteit en helderheid in organische lichtemitterende apparaten In welk jaar ontdekte Galileo Saturnus?
In welk jaar ontdekte Galileo Saturnus?  Hoeveel joules van warmte -energie worden vrijgegeven door elke gram waterdamp die condenseert om wolkdruppeltjes te vormen?
Hoeveel joules van warmte -energie worden vrijgegeven door elke gram waterdamp die condenseert om wolkdruppeltjes te vormen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

