
Wetenschap
Berekening van de zilverchlorideproductie uit de natriumchloridereactie
1. Schrijf de uitgebalanceerde chemische vergelijking:
NaCl (aq) + AgNO₃ (aq) → AgCl (s) + NaNO₃ (aq)
2. Bepaal de beperkende reactant:
Omdat we een teveel aan AgNO₃ hebben, is NaCl de beperkende reactant. Dit betekent dat de geproduceerde hoeveelheid AgCl wordt bepaald door de beschikbare hoeveelheid NaCl.
3. Bereken het aantal mol NaCl:
* Molaire massa van NaCl =58,44 g/mol
* Mol NaCl =(10 g) / (58,44 g/mol) =0,171 mol
4. Gebruik de molverhouding uit de uitgebalanceerde vergelijking om het aantal mol AgCl te vinden:
* De uitgebalanceerde vergelijking toont een molverhouding van 1:1 tussen NaCl en AgCl.
* Daarom zal 0,171 mol NaCl 0,171 mol AgCl produceren.
5. Bereken de massa van AgCl:
* Molaire massa van AgCl =143,32 g/mol
* Massa AgCl =(0,171 mol) * (143,32 g/mol) =24,5 g
Daarom wordt bij deze reactie 24,5 gram vast AgCl geproduceerd.
 Hong Kong bouwt kunstmatig eiland van $ 79 miljard
Hong Kong bouwt kunstmatig eiland van $ 79 miljard Smog keert terug naar Indiase hoofdstad nu landbouwbranden beginnen
Smog keert terug naar Indiase hoofdstad nu landbouwbranden beginnen Er moet rekening worden gehouden met zowel het potentieel als de beperkingen van herbebossing om de doelstellingen voor klimaatmitigatie te bereiken
Er moet rekening worden gehouden met zowel het potentieel als de beperkingen van herbebossing om de doelstellingen voor klimaatmitigatie te bereiken Tot de bodem van de afname van het zee-ijs in de Noordelijke IJszee:profilering van smeltwaterverdelingen om de voorspellingen van zee-ijs te versterken
Tot de bodem van de afname van het zee-ijs in de Noordelijke IJszee:profilering van smeltwaterverdelingen om de voorspellingen van zee-ijs te versterken De effecten van olieverontreiniging op aquatische ecosystemen
De effecten van olieverontreiniging op aquatische ecosystemen
Hoofdlijnen
- Welke carrières gebruiken wetenschappelijke notatie?
- Hoe cheeta's elkaar vinden na hun scheiding
- De eerste bloemen evolueerden vóór de bijen – dus hoe werden ze zo oogverblindend?
- Uit onderzoek blijkt dat de afkoeling van de oceaan gedurende millennia heeft geleid tot grotere vissen
- Wat is een basisverschil tussen protisten en schimmels?
- Wat is de structuur van homeostase?
- Welke producten ATP?
- Welke twee dingen vormen de ruggengraat van een DNA -molecuul?
- Grootschalig scherm laat zien hoe talloze signaalroutes elkaar kruisen in het primaire eiwitverwerkingscentrum van de cel
- Nieuwe techniek maakt snelle en goedkope productie van hoogwaardige circuits mogelijk

- Apparaatupdate maakt mobiel testen op virussen mogelijk, bacteriën en actieve toxines

- Geheimen van Lucretia schilderij dichter bij onthulling

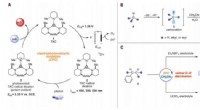
- Elektrofotokatalytische diaminatie van vicinale C-H-bindingen
- Een nieuw hulpmiddel voor cryo-elektronenmicroscopie

 Hoe beïnvloedt de wet van zwaartekracht objecten?
Hoe beïnvloedt de wet van zwaartekracht objecten?  De pH van een twee-chemisch mengsel berekenen
De pH van een twee-chemisch mengsel berekenen  Wat is de grootste cel die door het lichaam wordt geproduceerd?
Wat is de grootste cel die door het lichaam wordt geproduceerd?  Laatste mijlpaal voor de verbeterde H.E.S.S. telescopen in Namibië
Laatste mijlpaal voor de verbeterde H.E.S.S. telescopen in Namibië Toegepaste natuurkundigen creëren bouwstenen voor een nieuwe klasse optische circuits
Toegepaste natuurkundigen creëren bouwstenen voor een nieuwe klasse optische circuits Het verschil begrijpen tussen water- en luchtdruk
Het verschil begrijpen tussen water- en luchtdruk  De hittegolf in China drijft de prijzen op doordat kippen minder eieren leggen
De hittegolf in China drijft de prijzen op doordat kippen minder eieren leggen Wat maakt het ene materiaal een betere geleider dan de andere?
Wat maakt het ene materiaal een betere geleider dan de andere?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

