
Wetenschap
Koolwaterstofeigenschappen:hoe molecuulgrootte en atoomtelling er toe doen
Grootte (aantal koolstofatomen):
* Kookpunt en smeltpunt: Grotere koolwaterstoffen hebben sterkere London-dispersiekrachten (een soort intermoleculaire kracht) vanwege hun grotere oppervlak en meer elektronen. Dit resulteert in hogere kookpunten en smeltpunten. Zie het zo:grotere moleculen zijn moeilijker uit elkaar te trekken.
* Viscositeit: Grotere koolwaterstoffen zijn over het algemeen stroperiger (dikker). Dit is opnieuw te wijten aan sterkere intermoleculaire krachten.
* Ontvlambaarheid: Over het algemeen zijn kleinere koolwaterstoffen (zoals methaan en propaan) brandbaarder. Grotere koolwaterstoffen hebben meer energie nodig om te verdampen, waardoor ze minder snel ontbranden.
Aantal waterstofatomen:
* Verhouding waterstof/koolstof: De verhouding tussen waterstofatomen en koolstofatomen beïnvloedt de verzadiging van de koolwaterstof.
* Verzadigde koolwaterstoffen: Deze hebben het maximale aantal waterstofatomen dat mogelijk is voor het gegeven aantal koolstofatomen (bijvoorbeeld alkanen). Ze zijn doorgaans minder reactief.
* Onverzadigde koolwaterstoffen: Deze hebben minder waterstofatomen dan verzadigde koolwaterstoffen, wat leidt tot de aanwezigheid van dubbele of drievoudige bindingen (bijvoorbeeld alkenen, alkynen). Ze zijn over het algemeen reactiever.
Vertakking:
* Kookpunt en smeltpunt: Vertakte koolwaterstoffen hebben lagere kookpunten en smeltpunten dan hun tegenhangers met rechte keten. Dit komt omdat vertakkingen het beschikbare oppervlak voor Londense dispersiekrachten verkleinen.
* Viscositeit: Vertakte koolwaterstoffen zijn minder stroperig dan koolwaterstoffen met een rechte keten.
Voorbeelden:
* Methaan (CH4): Klein, licht ontvlambaar gas.
* Octaan (C8H18): Vloeistof, minder brandbaar dan methaan, gebruikt als benzine.
* Polyethyleen (C2H4)n: Polymeer met lange keten, vast bij kamertemperatuur, gebruikt voor plastic zakken.
Belangrijkste punten:
* De grootte van een koolwaterstofmolecuul bepaalt de sterkte van de intermoleculaire krachten, die het kookpunt, het smeltpunt en de viscositeit beïnvloeden.
* Het aantal waterstofatomen beïnvloedt de verzadiging en beïnvloedt de reactiviteit.
*Vertakkingen beïnvloeden het oppervlak en de intermoleculaire krachten, waardoor eigenschappen als kookpunt en viscositeit worden beïnvloed.
Algemeen: De eigenschappen van een koolwaterstof zijn een complex samenspel van de grootte, het aantal atomen en de structuur ervan. Het begrijpen van deze relaties helpt ons het gedrag van deze belangrijke verbindingen te voorspellen en te manipuleren.
 Nuttige microben inhaleren koolstofdioxide via een poreuze cilindrische elektrode en scheiden nuttige chemicaliën uit
Nuttige microben inhaleren koolstofdioxide via een poreuze cilindrische elektrode en scheiden nuttige chemicaliën uit Hoeveel elektronen zijn er op elke baan voor kalium?
Hoeveel elektronen zijn er op elke baan voor kalium?  Wat zijn de verschillende soorten niet -ferro -metalen?
Wat zijn de verschillende soorten niet -ferro -metalen?  Opsporen van vuilbronnen voor strafrechtelijk onderzoek
Opsporen van vuilbronnen voor strafrechtelijk onderzoek Wat is de molaire massa voor koper 2 chloride?
Wat is de molaire massa voor koper 2 chloride?
 Groot geologisch onderzoek hoopt Indonesië beter bestand te maken tegen dodelijke tsunami's
Groot geologisch onderzoek hoopt Indonesië beter bestand te maken tegen dodelijke tsunami's Gemeenschappen ontvluchten uitbarsting bij Vulkaan van Vuur in Guatemala
Gemeenschappen ontvluchten uitbarsting bij Vulkaan van Vuur in Guatemala Ecohydrologische modellering om bos- en graslandeffecten op waterscheiding en fluxleeftijden te kwantificeren
Ecohydrologische modellering om bos- en graslandeffecten op waterscheiding en fluxleeftijden te kwantificeren Fracking leidt waarschijnlijk tot hoge emissies
Fracking leidt waarschijnlijk tot hoge emissies Door de uitstoot geleidelijk te verminderen, wordt een plotselinge stijging van de opwarming voorkomen
Door de uitstoot geleidelijk te verminderen, wordt een plotselinge stijging van de opwarming voorkomen
Hoofdlijnen
- Wat is de relatie tussen biologie en fyschologie?
- Waarom hebben bladcellen zoveel bladgroenkorrels?
- Welke vier chemicaliën vormen de genetische code?
- Welk proces vindt plaats binnen de mesofylcellen van blad?
- Muizen helpen onderzoekers onderzoeken hoe het dieet van koeien het melkvetgehalte beïnvloedt
- Wat voor soort bacteriën groeien in water?
- Producten geproduceerd door Anaerobe ademhaling
- Factoren die het fenotype bepalen:genetica, omgeving en meer
- Waarom sommige mensen hun oren kunnen bewegen – de wetenschap achter de oorspieren
- Smaakonderzoek voor consumentenbescherming

- Make like a leaf:onderzoekers ontwikkelen methode om koolstofdioxide om te zetten

- Spontane synthese van homogene polymeernetwerken

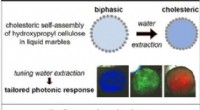
- Zelfassemblage van responsieve fotonische biobased materialen in vloeibare knikkers
- Wetenschappers hebben nieuwe verbindingen ontdekt met herbicide potentieel van zeeschimmel

 Welk mobiele telefoonsbedrijf biedt de gratis onbeperkte oproepen tussen 2 telefoons?
Welk mobiele telefoonsbedrijf biedt de gratis onbeperkte oproepen tussen 2 telefoons?  Studie van niet-regenwater in Namib Desert onthult onverwachte oorsprong
Studie van niet-regenwater in Namib Desert onthult onverwachte oorsprong Waarom ijs meestal bewolkt bevriest,
Waarom ijs meestal bewolkt bevriest,  Wat is een zonnetopee?
Wat is een zonnetopee?  Is de helft van de maan verlicht door de zon?
Is de helft van de maan verlicht door de zon?  Welk mineraal is plat met schilferige splitsing?
Welk mineraal is plat met schilferige splitsing?  Hoe zwaar water wordt gemaakt?
Hoe zwaar water wordt gemaakt?  Waarom fracken niet het antwoord is op de stijgende gasprijzen in het VK
Waarom fracken niet het antwoord is op de stijgende gasprijzen in het VK
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

