
Wetenschap
Enkele verplaatsingsreacties:Redox-processen begrijpen
* Redoxreacties: Deze reacties omvatten de overdracht van elektronen tussen reactanten. De ene reactant verliest elektronen (oxidatie), terwijl de andere elektronen wint (reductie).
* Enkele verplaatsingsreacties: Bij deze reacties verdringt een reactiever element een minder reactief element uit een verbinding. Deze verplaatsing vindt plaats omdat het meer reactieve element een sterkere neiging heeft om elektronen te verliezen (oxidatie) en het minder reactieve element een sterkere neiging heeft om elektronen te winnen (reductie).
Voorbeeld:
Beschouw de reactie van zink met koper(II)sulfaat:
Zn(s) + CuSO₄(aq) → ZnSO₄(aq) + Cu(s)
* Zink (Zn) is reactiever dan koper (Cu) .
* Zink verliest elektronen en wordt geoxideerd, waarbij Zn²⁺ ontstaat ionen.
* Koper(II)-ionen (Cu²⁺) krijgen elektronen en worden gereduceerd, waardoor kopermetaal (Cu) wordt gevormd .
Belangrijkste afhaalpunten: Omdat enkelvoudige verplaatsingsreacties een verandering in de oxidatietoestanden van de betrokken elementen met zich meebrengen, zijn het altijd redoxreacties.
 Hoe verschilt het samengestelde natriumchloride van elementen waarvan het samengesteld is?
Hoe verschilt het samengestelde natriumchloride van elementen waarvan het samengesteld is?  Het onvermengbare mengen:een nieuwe benadering voor het efficiënt samensmelten van verschillende polymeren
Het onvermengbare mengen:een nieuwe benadering voor het efficiënt samensmelten van verschillende polymeren Hoe beïnvloedt stroming de krachten van geladen oppervlakken/deeltjes en oppervlakteactieve stoffen in vloeistoffen?
Hoe beïnvloedt stroming de krachten van geladen oppervlakken/deeltjes en oppervlakteactieve stoffen in vloeistoffen?  Hoe Arsenic
Hoe Arsenic Lewis-puntstructuren voor O₂ en N₂:een stapsgewijze handleiding
Lewis-puntstructuren voor O₂ en N₂:een stapsgewijze handleiding
 Duurzame keuzes voor palmolie moeten voor de consument makkelijker worden, zegt nieuwe studie
Duurzame keuzes voor palmolie moeten voor de consument makkelijker worden, zegt nieuwe studie Wat at Megalodons naast de walvissen?
Wat at Megalodons naast de walvissen?  Waarom is een houtachtige oppervlakte van een boom altijd dikker dan dat zijn schors?
Waarom is een houtachtige oppervlakte van een boom altijd dikker dan dat zijn schors?  Nieuwe methode beoordeelt loodgevaar in bodem
Nieuwe methode beoordeelt loodgevaar in bodem Boeren vrezen dat het jaren zal duren om te herstellen van een stormstaking
Boeren vrezen dat het jaren zal duren om te herstellen van een stormstaking
Hoofdlijnen
- Wie is de wetenschapper ontdekt dat niet -virulente bacteriën zijn omgezet in virulente bacteriën?
- Is water een eencellulair organisme?
- Wat doen leukocyten?
- Wat heeft 1 cel of veel cellen?
- Welke term beschrijft de structuur van een celplasmamembraan omdat zijn olieachtige natuur ingebedde eiwitten heeft ingebed?
- Wat voor soort cel heeft een kern omringd door zijn eigen membraan en andere interne delen begrensde membranen?
- Welke groeimedia geven een rode kolonie van Escherechia coli?
- Nee,
- Wat is de functie van een contractiele vacuole in enkele geënte organismen?
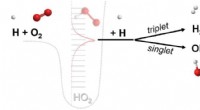
- IJzerkatalysator kan belangrijke chemische reacties goedkoper en milieuvriendelijker maken
- Positieve en negatieve ionen:hoe metalen en niet-metalen kationen en anionen vormen

- Onderzoekers ontdekken nieuwe klasse van chemische reacties
- Vooruitgang in superresolutiemicroscopie
- Met behulp van twee CRISPR-enzymen, een COVID-diagnose in slechts 20 minuten

 Hoe protectionisme ontwikkelingslanden kan helpen hun economisch potentieel te ontsluiten
Hoe protectionisme ontwikkelingslanden kan helpen hun economisch potentieel te ontsluiten  Herhaalt de oerknal zich?
Herhaalt de oerknal zich?  Is Diorite een grove korrelige rots?
Is Diorite een grove korrelige rots?  Golfsensoren ingezet om orkaanvoorspellingen te verbeteren
Golfsensoren ingezet om orkaanvoorspellingen te verbeteren Welk deel van een boom drinkt het water?
Welk deel van een boom drinkt het water?  Onderzoekers vinden aanwijzingen over hoe gevaarlijke ruimtestraling begint
Onderzoekers vinden aanwijzingen over hoe gevaarlijke ruimtestraling begint  2. Welk type energie zet een föhn om in thermische energie?
2. Welk type energie zet een föhn om in thermische energie?  Beste verklaring voor waarom Neiterkob de beginner van de aarde wordt genoemd?
Beste verklaring voor waarom Neiterkob de beginner van de aarde wordt genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

