
Wetenschap
Positieve en negatieve ionen:hoe metalen en niet-metalen kationen en anionen vormen
Door Carolyn LaRoche, bijgewerkt op 24 maart 2022
Sinhyu/iStock/GettyImages
Wat is een ion?
Atomen kunnen een elektrische lading verkrijgen door elektronen te verliezen of te winnen, waardoor ze ionen worden. Een positief geladen ion wordt een kation genoemd , terwijl een negatief geladen ion bekend staat als een anion . Ionen spelen een centrale rol bij de ionische binding, waardoor veel van de verbindingen ontstaan die we dagelijks tegenkomen.
Hoe ionen worden gevormd
Elk atoom bevat protonen (positief), neutronen (neutraal) en elektronen (negatief). Elektronen draaien rond de kern en kunnen tussen atomen bewegen. Wanneer een atoom één of meer elektronen verliest, wordt het een kation. Omgekeerd, wanneer een atoom elektronen verkrijgt, wordt het een anion. Het evenwicht tussen protonen en elektronen bepaalt de lading van het ion.
Kationen:positieve ionen uit metalen
Metalen, die het periodiek systeem domineren, verliezen gemakkelijk elektronen om een stabiele elektronenconfiguratie te bereiken. De resulterende kationen dragen doorgaans een positieve lading die overeenkomt met het aantal verloren elektronen. De lading varieert per metaalgroep:
- Groep 1 metalen (alkalimetalen) → +1
- Groepen 2, 12 en 16 → +2
- Groepen 13 en 15 → +3
- Groep 14 → +4
Omdat vrije elektronen overvloedig aanwezig zijn in metalen, geleiden ze elektriciteit efficiënt, een eigenschap die rechtstreeks verband houdt met de vorming van kationen.
Anionen:negatieve ionen van niet-metalen
Niet-metalen, gelegen aan de rechterkant van het periodiek systeem, hebben de neiging elektronen op te nemen om hun valentieschillen te vullen. Deze extra elektronen creëren een overschot aan negatieve lading en vormen anionen. De typische kosten zijn afhankelijk van de groep van het niet-metaal:
- Groepen 13 en 15 → –3
- Groep 14 → –4
- Groep 16 → –2
- Halogenen (Groep 17) → –1
In tegenstelling tot metalen geleiden niet-metalen geen elektriciteit omdat elektronen stevig aan hun atomen zijn gebonden.
Waarom dit belangrijk is
Het begrijpen van ionenvorming helpt bij het verklaren van een breed scala aan chemische verschijnselen, van hoe zout oplost in water tot hoe biologische cellen elektrische gradiënten in stand houden. Het herkennen van het ladingspatroon in het periodiek systeem helpt ook bij het voorspellen van het gedrag van elementen in chemische reacties.
 Voorstanders waaieren uit in een mondiale steunbetuiging voor de wetenschap
Voorstanders waaieren uit in een mondiale steunbetuiging voor de wetenschap  Hoe onze voedselkeuzes in bossen snijden en ons dichter bij virussen brengen
Hoe onze voedselkeuzes in bossen snijden en ons dichter bij virussen brengen Wateren voor de kust van New England in het midden van een recordjaar voor warmte
Wateren voor de kust van New England in het midden van een recordjaar voor warmte Steden in de cloud
Steden in de cloud Drie graden temperatuurstijging zal Europese inspanningen voor emissiereductie tenietdoen
Drie graden temperatuurstijging zal Europese inspanningen voor emissiereductie tenietdoen
Hoofdlijnen
- Waarom hebben alle cellen mitochondriën nodig?
- Hoe zijn bloemen vergelijkbaar met de voortplantingsorganen van de plant?
- Welke organel is een stapel membraneuze zakjes die betrokken zijn bij het sorteren van eiwitten op hun juiste cellulaire locatie?
- Wat zijn de producten en reactanten van cellulaire ademhaling waar komt het voor?
- Wat beschouwen wetenschappers waarschijnlijk als belangrijk bewijs bij het classificeren van een onbekend organisme?
- Wat is een trichomosoom?
- Stembesturing:waarom Noord-Atlantische walvissen van stem veranderen naarmate ze ouder worden
- Perzikperfectie:geavanceerde genennetwerken onthullen fruiteigenschappen
- Welke cellen bevatten geen DNA?
- Plastic afval omzetten in smeeroliën
- Winning van kostbare zeldzame-aarde-elementen uit steenkoolvliegas met een herbruikbare ionische vloeistof

- Het geheim van de Stradivari-viool bevestigd

- Hoe de topologie van een poreus materiaal de fasescheiding van binaire mengsels beïnvloedt

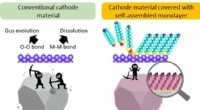
- Een betere batterij bouwen, laag voor laag
 Daalt de temperatuur van de aarde als u van korst naar kern beweegt?
Daalt de temperatuur van de aarde als u van korst naar kern beweegt?  Wat is de dichtheid van acrylplastic in Engelse eenheden?
Wat is de dichtheid van acrylplastic in Engelse eenheden?  Is er straling op de maan van de zon?
Is er straling op de maan van de zon?  Waarom vriendschappen uit elkaar vallen door politiek
Waarom vriendschappen uit elkaar vallen door politiek Wat was theorie over evolutie?
Wat was theorie over evolutie?  Waarom wordt de temperatuur hoger?
Waarom wordt de temperatuur hoger?  Niet op schaal? Maya-beschavingen vertonen een vreemde correlatie
Niet op schaal? Maya-beschavingen vertonen een vreemde correlatie  Hoe kun je een relatieve vochtigheid gebruiken?
Hoe kun je een relatieve vochtigheid gebruiken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

