
Wetenschap
Kaliumhydroxide- en zoutzuurreactie:een gedetailleerde uitleg
Hier is de uitsplitsing:
* Reactie: KOH (aq) + HCl (aq) → KCl (aq) + H₂O (l)
* Uitleg:
* Kaliumhydroxide (KOH) is een sterke base, wat betekent dat het in oplossing gemakkelijk dissocieert in kaliumionen (K⁺) en hydroxide-ionen (OH⁻).
* Zoutzuur (HCl) is een sterk zuur, wat betekent dat het in oplossing gemakkelijk dissocieert in waterstofionen (H⁺) en chloride-ionen (Cl⁻).
* Wanneer deze oplossingen worden gemengd, reageren de waterstofionen (H⁺) uit het zuur met de hydroxide-ionen (OH⁻) uit de base om water (H₂O) te vormen.
* De overige ionen, kaliumionen (K⁺) en chloride-ionen (Cl⁻), vormen samen kaliumchloride (KCl), een zout dat opgelost blijft in de oplossing.
Resultaat:
* De reactie produceert warmte (exotherme reactie) terwijl de ionen zich binden en water en zout vormen.
* De resulterende oplossing is neutraal , wat betekent dat het een pH heeft die dichtbij 7 ligt.
* Het gevormde zout, kaliumchloride (KCl), is een oplosbare ionische verbinding die opgelost blijft in het water.
Belangrijke opmerking:
* Deze reactie is zeer exotherm. Het mengen van geconcentreerde oplossingen kan aanzienlijke hitte genereren, wat mogelijk spatten of zelfs koken kan veroorzaken. Voeg de base altijd langzaam en onder voortdurend roeren aan het zuur toe om de gegenereerde warmte onder controle te houden.
* Dit is een veel voorkomende laboratoriumreactie die wordt gebruikt voor titraties en andere chemische experimenten.
 Welk element heeft eigenschappen vergelijkbaar met chloor en fluor?
Welk element heeft eigenschappen vergelijkbaar met chloor en fluor?  Is BAF2 een ionische of covalente binding?
Is BAF2 een ionische of covalente binding?  Nieuwe tool kan schadelijke blauwgroene algen identificeren
Nieuwe tool kan schadelijke blauwgroene algen identificeren Onderzoekers bestuderen historische ontwikkelingen van het periodiek systeem van chemische elementen
Onderzoekers bestuderen historische ontwikkelingen van het periodiek systeem van chemische elementen Een nieuwe workflow voor statistische modellen kan de ontdekking van geneesmiddelen en de synthetische chemie helpen bevorderen
Een nieuwe workflow voor statistische modellen kan de ontdekking van geneesmiddelen en de synthetische chemie helpen bevorderen
 Wat is het punt waarover bomen niet kunnen groeien?
Wat is het punt waarover bomen niet kunnen groeien?  Hoe je genuanceerde details krijgt aan de top van de wereld
Hoe je genuanceerde details krijgt aan de top van de wereld Hoe het wordt in de wetenschap genoemd wanneer conclusie uit een observatie ontstaat?
Hoe het wordt in de wetenschap genoemd wanneer conclusie uit een observatie ontstaat?  Kan water of lucht door hout passeren?
Kan water of lucht door hout passeren?  De temperaturen in het noordoosten van de VS liggen tientallen jaren hoger dan het wereldwijde gemiddelde
De temperaturen in het noordoosten van de VS liggen tientallen jaren hoger dan het wereldwijde gemiddelde
Hoofdlijnen
- Welke structuur is verantwoordelijk voor het synthetiseren van eiwitten?
- Wat is het centrale idee van evolutie?
- Studie onthult onderliggende genetische basis voor communicatie en sociaal gedrag van halictidebijen
- Wat is het niveau van levende organismen in orde van het kleinste tot de grootste?
- Leeft Silex Strobilus als het op koolstof gebaseerd is voldoende om een groot molecuul te hebben dat zelfreplicaties zijn Bewegend organisme?
- Selecteer alles wat van toepassing is. Welke kenmerken hebben archaea en bacteriën gemeen?
- Welk proces stelt cellen in staat om naar de cel te gaan zonder gebruik van chemische energie?
- Wat is de belangrijkste familie van voedselproducerende planten?
- Wat is een ectoderm in de embryologie?
- Onderzoekers identificeren enzym dat verantwoordelijk is voor de verspreiding van kankertumoren

- Onaangename geuren uit het airconditioningsysteem van uw auto identificeren en oplossen
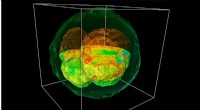
- Nieuwe microscooptechniek onthult interne structuur van levende embryo's
- Wetenschappers vinden sneller uit, goedkopere strategie voor het ontwerpen van infrarood-emitterende materialen

- Verbeterde sterkte en taaiheid in een legering met hoge entropie via geordende zuurstofcomplexen
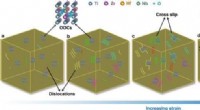
 Wat is energie in bewegende dingen die worden genoemd?
Wat is energie in bewegende dingen die worden genoemd?  2 kiwivogels zijn zeldzaam lichtpuntje in grimmig uitstervingsrapport
2 kiwivogels zijn zeldzaam lichtpuntje in grimmig uitstervingsrapport Welke compound bevat voedsel als het zwart wordt wanneer het wordt getest met jodium?
Welke compound bevat voedsel als het zwart wordt wanneer het wordt getest met jodium?  Vlinders, bijen, insecten en meer:de zomer van het tellen van insecten begint in Duitsland
Vlinders, bijen, insecten en meer:de zomer van het tellen van insecten begint in Duitsland  Micron investeert $ 15 miljard in geheugenchipfabriek in Boise
Micron investeert $ 15 miljard in geheugenchipfabriek in Boise Waar is wetenschappelijke metingen op gebaseerd?
Waar is wetenschappelijke metingen op gebaseerd?  Wat zijn de deelnemers aan fotosynthese?
Wat zijn de deelnemers aan fotosynthese?  Waarom zijn gassen goede isolatoren?
Waarom zijn gassen goede isolatoren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

