
Wetenschap
'Like Dissolves Like' begrijpen:polariteit en oplosbaarheid in de chemie
Like lost Like op:een nadere blik
De regel 'het gelijke lost het gelijke op' is een fundamenteel principe in de scheikunde, vooral bij het begrijpen van de oplosbaarheid van stoffen. Het stelt in wezen dat stoffen met vergelijkbare polariteiten de neiging hebben om in elkaar op te lossen.
Polariteit en oplosbaarheid:
* Polariteit verwijst naar de verdeling van elektrische lading binnen een molecuul. Polaire moleculen hebben een positief en een negatief uiteinde, waardoor een dipoolmoment ontstaat. Voorbeelden hiervan zijn water (H₂O) en ethanol (CH₃CH₂OH).
* Niet-polair moleculen hebben een gelijkmatige ladingsverdeling, zonder duidelijke positieve of negatieve uiteinden. Voorbeelden hiervan zijn olie en vet.
Hoe de regel werkt:
* Polaire oplosmiddelen polaire opgeloste stoffen oplossen . Dit komt omdat het positieve uiteinde van het oplosmiddelmolecuul kan interageren met het negatieve uiteinde van het opgeloste molecuul, en omgekeerd, waardoor sterke aantrekkingen ontstaan.
* Niet-polaire oplosmiddelen niet-polaire opgeloste stoffen oplossen . De krachten die deze moleculen bij elkaar houden zijn zwakke Van der Waals-krachten. Soortgelijke krachten bestaan tussen het oplosmiddel en de opgeloste moleculen, waardoor ze zich kunnen vermengen.
Bijdrage van de structuur:
De structuur van een molecuul speelt een cruciale rol bij het bepalen van de polariteit en dus de oplosbaarheid ervan. Hier ziet u hoe:
* Functionele groepen: Verschillende functionele groepen binnen een molecuul dragen bij aan de polariteit ervan. De aanwezigheid van een hydroxylgroep (-OH) in ethanol maakt het bijvoorbeeld polair, terwijl de afwezigheid van dergelijke groepen in koolwaterstoffen ze niet-polair maakt.
* Moleculaire vorm: De vorm van een molecuul kan de interacties met andere moleculen beïnvloeden. Lineaire moleculen zijn doorgaans polairder dan vertakte moleculen.
* Intermoleculaire krachten: Het type en de sterkte van de intermoleculaire krachten die in een molecuul aanwezig zijn, spelen ook een rol bij de oplosbaarheid. Polaire moleculen hebben sterkere dipool-dipoolinteracties, terwijl niet-polaire moleculen zwakkere London-dispersiekrachten hebben.
Voorbeelden:
* Water (polair oplosmiddel) lost suiker (polaire opgeloste stof) op, maar olie (niet-polaire opgeloste stof) niet. De polaire watermoleculen kunnen sterke waterstofbruggen vormen met de polaire suikermoleculen, wat tot ontbinding leidt.
* Olie (niet-polair oplosmiddel) lost vet (niet-polaire opgeloste stof) op, maar zout niet (polaire opgeloste stof). De niet-polaire oliemoleculen kunnen via zwakke Van der Waals-krachten een interactie aangaan met de niet-polaire vetmoleculen.
Uitzonderingen:
* Amfifiele moleculen: Deze moleculen hebben zowel polaire als niet-polaire gebieden. Zeepmoleculen hebben bijvoorbeeld een polaire kop en een niet-polaire staart. Ze kunnen zowel polaire als niet-polaire stoffen oplossen.
* Waterstofbinding: Moleculen die waterstofbruggen kunnen vormen (zoals water) kunnen soms moleculen oplossen die niet strikt polair zijn, maar toch via waterstofbruggen met water kunnen interageren.
Samenvattend:
De regel 'het gelijke lost het gelijke op' is een nuttige leidraad, maar het is belangrijk om te onthouden dat het geen vaste regel is. Structuur, intermoleculaire krachten en andere factoren spelen ook een belangrijke rol bij het bepalen van de oplosbaarheid. Door deze factoren te begrijpen, kunnen we de oplosbaarheid van verschillende stoffen beter voorspellen en verklaren.
 Wat zijn geïoniseerde druppels?
Wat zijn geïoniseerde druppels?  Goud en zoutzuur:chemische reactie en waarom goud niet oplost
Goud en zoutzuur:chemische reactie en waarom goud niet oplost  Chemici doen historische ontdekking van fluor
Chemici doen historische ontdekking van fluor Waarom is cyclohexylamine sterker dan aniline?
Waarom is cyclohexylamine sterker dan aniline?  Machine learning biedt een snelkoppeling om interacties in materialen te simuleren voor het oogsten van zonne-energie
Machine learning biedt een snelkoppeling om interacties in materialen te simuleren voor het oogsten van zonne-energie
 Hoe het nieuwe mensenrecht op een gezond milieu de actie van Nieuw-Zeeland op het gebied van klimaatverandering kan versnellen
Hoe het nieuwe mensenrecht op een gezond milieu de actie van Nieuw-Zeeland op het gebied van klimaatverandering kan versnellen Deze kleine oceanische wezens zijn essentieel om de klimaatverandering aan te pakken
Deze kleine oceanische wezens zijn essentieel om de klimaatverandering aan te pakken Florida wacht:orkaan Dorian ziet er steeds grimmiger uit
Florida wacht:orkaan Dorian ziet er steeds grimmiger uit Wolk verhelderend, zonneschermen om Barrier Reef te redden
Wolk verhelderend, zonneschermen om Barrier Reef te redden Tarwe en bankgras kunnen giftige metalen uit verontreinigde grond halen
Tarwe en bankgras kunnen giftige metalen uit verontreinigde grond halen
Hoofdlijnen
- Welke verbinding wordt tijdens regeneratie geproduceerd?
- Worden de sporen geproduceerd door mos sporophyt gevormd meiose of mitose?
- De wetenschappelijke methode kan het beste worden omschreven als een plan of set van.
- Wie zijn de beroemde bioloog en wat hun bijdragen?
- Wat zijn de vijf basisgroep van micro -organismen?
- Hoe u uw bloedgroep kunt afleiden uit de bloedgroepen van uw ouders
- Waarom hebben de nieren de vorm van bonen?
- Welke functie hebben co-enzymen bij de ademhaling?
- Wat zijn de vier stikstofhoudende bases van DNA?
- Maak een realistisch aluminiumatoommodel voor klassikaal leren

- Kleine aminozuurverschillen kunnen leiden tot dramatisch verschillende enzymen
- Ingenieurs introduceren een nieuwe aanpak voor het recyclen van kunststoffen

- Waterafstotend materiaal werpt af als een slang bij beschadiging

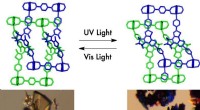
- Nieuw flexibel materiaal verandert zijn poreuze aard bij blootstelling aan licht
 Hematietrijke afzettingen in Capri Chasma
Hematietrijke afzettingen in Capri Chasma Een kijkje in wat NASA's nieuwe rover voor Mars heeft ingepakt
Een kijkje in wat NASA's nieuwe rover voor Mars heeft ingepakt  Reynolds Aluminiumfolie Wetenschapsprojecten
Reynolds Aluminiumfolie Wetenschapsprojecten Wat is beweging van een lichaamsdeel naar de hoofdas die wordt genoemd?
Wat is beweging van een lichaamsdeel naar de hoofdas die wordt genoemd?  Wat gebeurt er 's nachts met bijen en wespen?
Wat gebeurt er 's nachts met bijen en wespen?  Geef een voorbeeld van de chemische formule een samenstelling Wat vertelt dit u over verbinding?
Geef een voorbeeld van de chemische formule een samenstelling Wat vertelt dit u over verbinding?  China richt zich op afhaalcontainers om plastic afval te verminderen
China richt zich op afhaalcontainers om plastic afval te verminderen Is de verwarmingssnelheid gelijk aan het afkoelen van een stof?
Is de verwarmingssnelheid gelijk aan het afkoelen van een stof?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

