
Wetenschap
Elektrische geleidbaarheid van ionische en covalente verbindingen:staatsafhankelijkheid
Ionische verbindingen
* Solid State: Doe niet elektriciteit geleiden. De ionen worden stevig vastgehouden in een kristalrooster en kunnen niet vrij bewegen.
* Vloeibare toestand (gesmolten) :Gedrag elektriciteit. Wanneer ze gesmolten zijn, kunnen de ionen vrij bewegen en de elektrische stroom transporteren.
* Waterige oplossing: Gedrag elektriciteit. Wanneer ze in water worden opgelost, dissociëren de ionen en worden ze mobiel, waardoor elektrische geleiding mogelijk is.
Covalente verbindingen
* Solid State: De meeste niet elektriciteit geleiden. Covalente verbindingen delen elektronen, en deze elektronen zijn doorgaans gelokaliseerd in de bindingen en kunnen niet vrij bewegen.
* Vloeibare toestand: De meeste niet elektriciteit geleiden. Net als in de vaste toestand zijn de elektronen nog steeds grotendeels gelokaliseerd in de bindingen.
* Waterige oplossing: Sommigen doen geleiden elektriciteit, maar alleen als ze polair zijn en ioniseren in water. Dit komt omdat het ionisatieproces ionen creëert die vervolgens de stroom kunnen transporteren. Zoutzuur (HCl) lost bijvoorbeeld op in water en vormt H+- en Cl-ionen, waardoor het geleidend wordt.
Samengevat:
* Ionische verbindingen geleiden elektriciteit in hun gesmolten toestand en in waterige oplossingen .
* Covalente verbindingen geleiden over het algemeen geen elektriciteit, behalve polaire covalente verbindingen die in water ioniseren.
Opmerking: Er zijn enkele uitzonderingen op deze algemene regels. Grafiet, een vorm van koolstof, is bijvoorbeeld een covalente verbinding die vanwege zijn unieke structuur elektriciteit in vaste toestand kan geleiden.
 Welke is een binaire samengestelde waterstofsulfidesulfidesulfaat ammonium of sulfaat?
Welke is een binaire samengestelde waterstofsulfidesulfidesulfaat ammonium of sulfaat?  Sterke coördinatie-interactie geïdentificeerd als gunstig voor het bevorderen van dehydrogenering van ethanol
Sterke coördinatie-interactie geïdentificeerd als gunstig voor het bevorderen van dehydrogenering van ethanol  Bepaling van de kristalstructuur van een DNA-gestabiliseerd zilveren nanocluster
Bepaling van de kristalstructuur van een DNA-gestabiliseerd zilveren nanocluster Met behulp van 'donkere kanaal'-fluorescentie leggen wetenschappers uit hoe biochemische stoffen hun functie uitoefenen
Met behulp van 'donkere kanaal'-fluorescentie leggen wetenschappers uit hoe biochemische stoffen hun functie uitoefenen  Snel 3D-printen met zichtbaar licht
Snel 3D-printen met zichtbaar licht
 Waarom zijn er geen wettelijke beschermingen voor de kinderen van influencers?
Waarom zijn er geen wettelijke beschermingen voor de kinderen van influencers?  Een recente ommekeer in de reactie van de ijskappen in West-Groenland op klimaatverandering
Een recente ommekeer in de reactie van de ijskappen in West-Groenland op klimaatverandering Het ecosysteem van Mozambique
Het ecosysteem van Mozambique Een miljoen jaar neerslaggeschiedenis van de moesson gereconstrueerd
Een miljoen jaar neerslaggeschiedenis van de moesson gereconstrueerd Met de hand droge toiletten bouwen in de kustdorpen van Papoea-Nieuw-Guinea om de gevolgen van klimaatverandering tegen te gaan
Met de hand droge toiletten bouwen in de kustdorpen van Papoea-Nieuw-Guinea om de gevolgen van klimaatverandering tegen te gaan
Hoofdlijnen
- Wanneer gespecialiseerde tijdschriften waarin wetenschappers de resultaten van hun werken publiceren worden genoemd?
- Hoe noemen wetenschappers de aliens en vreemde organismen die onder de bodem van leven?
- Wat is een bewijs voor evolutie?
- Wie heeft klonen bedacht en wanneer?
- Hebben alle planten- en diercellen pili?
- Wat is iets dat dezelfde functie vervult als nucleolus in de cel?
- Wat is het proces waarin bacteriestukken DNA uit hun omgeving verhogen?
- Hoe brassinosteroïde-signalering ervoor zorgt dat wortels langer groeien onder stikstofgebrek
- Geven mensen overal minder om hun katten dan om honden?
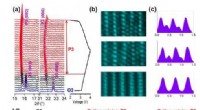
- Kationmenging induceert zeer efficiënte natriumopslag voor gelaagde kathoden
- James A. Harris:de Afro-Amerikaanse pionier achter de ontdekking van Rutherfordium en Dubnium

- Alles-afstotende coating kan telefoons kinderveilig maken, huizen

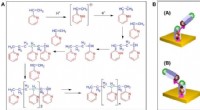
- Een chiraal polymeer maken van achirale monomeren met behulp van een magnetisch veld
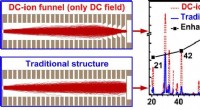
- Verbetering van de efficiëntie van de ionentransmissie van massaspectrometers
 Onderzoekers vinden de richting bepaald door de snelheid van het opgooien van munten in de kwantumwereld
Onderzoekers vinden de richting bepaald door de snelheid van het opgooien van munten in de kwantumwereld Hoe de dood van voicemail de manier waarop we verbinding maken verandert
Hoe de dood van voicemail de manier waarop we verbinding maken verandert Welke verbinding biedt het reducerende vermogen voor Calvin -cyclusreacties?
Welke verbinding biedt het reducerende vermogen voor Calvin -cyclusreacties?  Waarom zien we Proxima Centauri in de lucht?
Waarom zien we Proxima Centauri in de lucht?  Wetenschappers ontwikkelen nieuwe chip voor snelle en nauwkeurige ziektedetectie tegen lage kosten
Wetenschappers ontwikkelen nieuwe chip voor snelle en nauwkeurige ziektedetectie tegen lage kosten Kunnen twee soorten verschillende niches en dezelfde habitat bezetten?
Kunnen twee soorten verschillende niches en dezelfde habitat bezetten?  Het einde van de zon is geleidelijk en niet catastrofaal:wat gebeurt er de komende 10 miljard jaar
Het einde van de zon is geleidelijk en niet catastrofaal:wat gebeurt er de komende 10 miljard jaar  Is Betelgeuse in de Melkweg Galaxy?
Is Betelgeuse in de Melkweg Galaxy?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

