
Wetenschap
Oplosbaarheid begrijpen:waarom stoffen oplossen
1. Intermoleculaire krachten:
* Interacties tussen oplosmiddelen en opgeloste stoffen: De oplosmiddelmoleculen moeten een sterke aantrekkingskracht hebben op de opgeloste moleculen. Deze aantrekkingskracht is gebaseerd op intermoleculaire krachten zoals waterstofbruggen, dipool-dipoolinteracties of Londense dispersiekrachten.
* Interacties tussen opgeloste stoffen: De opgeloste moleculen moeten van elkaar kunnen loskomen. Als de opgeloste moleculen te sterk tot elkaar worden aangetrokken, kunnen ze niet oplossen.
2. Polariteit:
* Like lost op als: Dit is een veelgebruikt gezegde in de scheikunde. Polaire oplosmiddelen (zoals water) hebben de neiging om polaire opgeloste stoffen (zoals suiker) op te lossen, terwijl niet-polaire oplosmiddelen (zoals olie) de neiging hebben om niet-polaire opgeloste stoffen (zoals vet) op te lossen.
3. Entropie:
* Toegenomen stoornis: Wanneer een opgeloste stof oplost, raakt deze meer verspreid in het oplosmiddel, wat leidt tot een toename van de entropie (stoornis) van het systeem. Deze toename van de entropie bevordert het oplosproces.
4. Temperatuur:
* Hogere temperaturen bevorderen over het algemeen het oplossen: Een hogere temperatuur levert meer energie op om de intermoleculaire krachten die de opgeloste stof bij elkaar houden te overwinnen en zorgt ervoor dat de oplosmiddelmoleculen sneller kunnen bewegen, waardoor de interacties met de opgeloste stof toenemen.
5. Druk:
* Druk heeft vooral invloed op het oplossen van gassen in vloeistoffen: Verhoogde druk dwingt meer gasmoleculen tot oplossing. Daarom lost koolstofdioxide onder hogere druk beter op in frisdrank.
Voorbeeld:
* Suiker die oplost in water: Suiker is een polair molecuul en water is een polair oplosmiddel. De waterstofbinding tussen watermoleculen en de hydroxylgroepen in suiker zorgt voor sterke interacties tussen oplosmiddelen en opgeloste stoffen. De suikermoleculen hebben ook voldoende energie om van elkaar los te breken, waardoor ze omringd kunnen worden door watermoleculen en oplossen.
Samengevat:
Een stof kan in een andere stof worden opgelost als de oplosmiddelmoleculen een sterke aantrekkingskracht hebben op de opgeloste moleculen, de opgeloste moleculen van elkaar kunnen loskomen en het algehele proces leidt tot een toename van de entropie. De polariteit van het oplosmiddel en de opgeloste stof, evenals de temperatuur en druk, spelen ook een belangrijke rol.
 Permacultuur heeft ons laten zien hoe we het land zachter kunnen bewerken. Kunnen we hetzelfde doen als de zee?
Permacultuur heeft ons laten zien hoe we het land zachter kunnen bewerken. Kunnen we hetzelfde doen als de zee?  Grotere delen tropisch bos gaan verloren aan commerciële landbouw
Grotere delen tropisch bos gaan verloren aan commerciële landbouw Nieuwste klimaatmodellen laten meer intense droogte zien
Nieuwste klimaatmodellen laten meer intense droogte zien Seismologen bezorgd over bevingen in DR Congo
Seismologen bezorgd over bevingen in DR Congo India zegt dat Chinese constructie op rivier het water vervuilt
India zegt dat Chinese constructie op rivier het water vervuilt
Hoofdlijnen
- Onderzoekers suggereren dat mechanische druk een belangrijke gebeurtenis in de HIV-infectie veroorzaakt
- Hoe kunnen structuren in cel de gespecialiseerde zijn?
- Welke bloem draagt de zaden mannelijk of vrouwelijk?
- Is er een mogelijkheid dat vertaling eerst plaatsvindt vóór transcriptie?
- Waarom scheiden cellen naarmate een organisme groeit?
- Wat zijn 4 stukken bewijsevolutie?
- Wat is Saccharephidrosis?
- Welke eerste stappen hebben wetenschappers genomen om transgene bacteriën te produceren die insuline hebben gemaakt?
- Wat is Biogaster?
- Katalysatoren gevonden om koolstofdioxide om te zetten in brandstof

- Video:Wat doen rechercheurs op de plaats delict eigenlijk?

- Nieuwe aanpak creëert een uitzonderlijke katalysator met één atoom voor watersplitsing

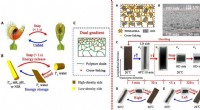
- Ontwikkeling van een ultrasnel biomimetisch snapping hydrogelmateriaal met twee gradiënten
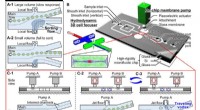
- Baanbrekende zuivering van fossiel stuifmeel met behulp van een nieuwe on-chip sorter voor grote deeltjes
 Een nieuw wapen tegen malaria:wetenschappers hebben een nieuw doelwit ontdekt om de verantwoordelijke parasiet te blokkeren
Een nieuw wapen tegen malaria:wetenschappers hebben een nieuw doelwit ontdekt om de verantwoordelijke parasiet te blokkeren Wat is een vaste snelheid?
Wat is een vaste snelheid?  Kan de overgebleven warmte van de laatste El Nino een nieuwe brandstof opleveren?
Kan de overgebleven warmte van de laatste El Nino een nieuwe brandstof opleveren? Welk type Earth Biome bezet de grootste gebieds aarde?
Welk type Earth Biome bezet de grootste gebieds aarde?  Studie vindt geen versnelling in misdaad van Formule 1-race
Studie vindt geen versnelling in misdaad van Formule 1-race Wat is plasmide en welk voordeel kan een bacterie krijgen door er een te verwerven?
Wat is plasmide en welk voordeel kan een bacterie krijgen door er een te verwerven?  Wat zijn giftige gassen?
Wat zijn giftige gassen?  Waar bevindt Chamaeleon zich in de lucht?
Waar bevindt Chamaeleon zich in de lucht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

