
Wetenschap
De effecten van onvoldoende zuur bij neutralisatie begrijpen
* Onvolledige neutralisatie: Het zuur zal slechts gedeeltelijk reageren met de alkali. Dit betekent dat niet alle alkali zal worden geneutraliseerd en dat de oplossing basisch zal blijven.
* pH blijft boven 7: De pH van de oplossing zal nog steeds groter zijn dan 7, wat wijst op een basische oplossing.
* Geen significante verandering in eigenschappen: Mogelijk merkt u geen dramatische verandering in de eigenschappen van de oplossing. Als u bijvoorbeeld een sterke base zoals natriumhydroxide (NaOH) probeert te neutraliseren, zal de oplossing waarschijnlijk nog steeds glad aanvoelen en nog steeds huidirritatie veroorzaken.
Voorbeeld:
Stel je voor dat je een oplossing van natriumhydroxide (NaOH) probeert te neutraliseren met zoutzuur (HCl). Als je te weinig HCl toevoegt, is de reactie:
NaOH + HCl → NaCl + H2 O
Maar omdat je niet genoeg HCl hebt toegevoegd, zal er nog steeds wat niet-gereageerd NaOH in de oplossing achterblijven, waardoor deze basisch blijft.
Belangrijke opmerking: Het is van cruciaal belang om te begrijpen dat de hoeveelheid zuur die nodig is om een alkali volledig te neutraliseren, afhangt van de specifieke stoffen die erbij betrokken zijn en hun concentraties. Raadpleeg altijd stoichiometrie en overweeg het gebruik van een pH-meter of indicator om het eindpunt van de reactie te bepalen.
 Is BaCl2 en zuur of base?
Is BaCl2 en zuur of base?  Wat zijn de essentiële grondstoffen die nodig zijn voor fotosynthese?
Wat zijn de essentiële grondstoffen die nodig zijn voor fotosynthese?  Hoe u de verbrandingswarmte van paraffinewas kunt meten:een stapsgewijze handleiding voor calorimetrie
Hoe u de verbrandingswarmte van paraffinewas kunt meten:een stapsgewijze handleiding voor calorimetrie  Gebruik van aluminiumhydroxide:toepassingen en voordelen in verschillende industrieën
Gebruik van aluminiumhydroxide:toepassingen en voordelen in verschillende industrieën  Welke ionen vormen de samengestelde PBCL4?
Welke ionen vormen de samengestelde PBCL4?
 Pakistan gaat tegen de stroom in met kolenstroom
Pakistan gaat tegen de stroom in met kolenstroom Aardbeving op Grieks eiland Kreta doodt één, zaait paniek
Aardbeving op Grieks eiland Kreta doodt één, zaait paniek NASA's tijdelijke controle op tropische storm Belna vindt potentieel voor zware regenval
NASA's tijdelijke controle op tropische storm Belna vindt potentieel voor zware regenval Waarom wordt een Firefly gezegd dat het een natuurlijke bron van licht is?
Waarom wordt een Firefly gezegd dat het een natuurlijke bron van licht is?  Wat is een standpunt waarin je dingen in de naam Wetenschap hebt genoemd?
Wat is een standpunt waarin je dingen in de naam Wetenschap hebt genoemd?
Hoofdlijnen
- Nieuwe ontdekking daagt lang gekoesterde evolutietheorie uit
- Onderzoekers bestuderen hoe genetische stoornissen zich ontwikkelen – in een petrischaaltje (met video)
- Wie is de wetenschapper die cellen voor het eerst beschreef?
- Welke van deze organellen in de krachtpatsercel?
- Welke verklaring beschrijft biostimulatie het beste?
- Welk element van het wetenschappelijke proces kan niet worden gewijzigd?
- De aandelen van Facebook zinken, dus wie moet het kopen?
- Welke zuren kunnen worden gevonden bij mensenlichaam?
- Wespengif bevat aanwijzingen over hoe genen nieuwe banen krijgen
- Natuurkunde versus astma

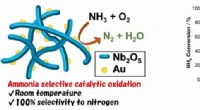
- Doorbraak in luchtzuivering met een katalysator die werkt bij kamertemperatuur
- Onderzoekers ontwikkelen nieuwe methode voor levering van glucagon

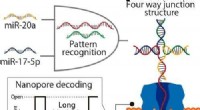
- Nanopore-technologie met DNA-computing detecteert gemakkelijk microRNA-patronen van longkanker
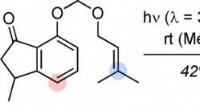
- Totale synthese van de sesquiterpeen agarozizanol B
 Hoe heet de meest primitieve bacteriën?
Hoe heet de meest primitieve bacteriën?  Wat is de naam van het object dat wordt gegeven aan Force die eerst op een tweede object wordt uitgeoefend?
Wat is de naam van het object dat wordt gegeven aan Force die eerst op een tweede object wordt uitgeoefend?  Hoge ijskliffen kunnen grote afkalvingsgebeurtenissen veroorzaken - en snelle zeespiegelstijging
Hoge ijskliffen kunnen grote afkalvingsgebeurtenissen veroorzaken - en snelle zeespiegelstijging Schaarse metalen die niet worden teruggewonnen uit autowrakken
Schaarse metalen die niet worden teruggewonnen uit autowrakken Extrusieve stollingsrotsen vormen zich wanneer ze harden en koelt.
Extrusieve stollingsrotsen vormen zich wanneer ze harden en koelt.  Welke energie -veranderingen vinden plaats als de jongen voetbal schopt?
Welke energie -veranderingen vinden plaats als de jongen voetbal schopt?  Welke Amerikaanse staat kan een persoon bezoeken om gematigde loofvetten te zien omringd door zout water aan 3 zijden?
Welke Amerikaanse staat kan een persoon bezoeken om gematigde loofvetten te zien omringd door zout water aan 3 zijden?  Waarom heeft zwaveldhexafluoride een laag kookpunt?
Waarom heeft zwaveldhexafluoride een laag kookpunt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

