
Wetenschap
Ionisatie-energie:identificatie van het atoom met de laagste elektronenverwijderingsenergie
* Ionisatie-energie: De energie die nodig is om het meest losjes gebonden elektron uit een gasvormig atoom te verwijderen, wordt ionisatie-energie genoemd.
* Periodieke trends: De ionisatie-energie neemt over het algemeen toe naarmate u beweegt:
* Over een periode (van links naar rechts): Atomen hebben een sterkere greep op hun elektronen als gevolg van de toenemende nucleaire lading.
* Een groep omhoog (van boven naar beneden): Elektronen bevinden zich verder van de kern, waardoor ze gemakkelijker te verwijderen zijn.
Laten we de opties analyseren:
* Sn (Tin): Groep 14, Periode 5
* Sr (Strontium): Groep 2, Periode 5
* Wees (Beryllium): Groep 2, Periode 2
* Br (Broom): Groep 17, Periode 4
Redenering:
* Strontium (Sr) en Beryllium (Be): Beide bevinden zich in Groep 2 (aardalkalimetalen). Sr bevindt zich verder in de groep dan Be, dus het buitenste elektron bevindt zich verder van de kern en is gemakkelijker te verwijderen.
* Tin (Sn) en broom (Br): Sn zit in Groep 14, Br zit in Groep 17. Broom zal een hogere ionisatie-energie hebben vanwege zijn grotere nucleaire lading en sterkere aantrekkingskracht op zijn elektronen.
Conclusie:
Gebaseerd op periodieke trends, Strontium (Sr) vereist de minste energie om het meest losjes gebonden elektron te verwijderen.
Daarom is het antwoord (b).
Hoofdlijnen
- Wat is de belangrijkste functie van plasmacelmembraan in een plantencel?
- Wat wordt er geproduceerd in de speekselklieren?
- Wat zijn voordeel en nadeel van de moderne biotechnologie?
- Waarom wordt gezegd dat bladeren excretoforen zijn?
- Wat voor soort vlekken worden gebruikt om cellen te planten en dieren?
- Twee soorten Cilia in een Paramecium
- Vrijlating van hagedissen brengt zeldzame soorten terug naar hun natuurlijke habitat in Groot-Brittannië
- Wat is de reden voor hemiparese?
- Wat is een voorbeeld van een meercellige schimmels?
- Nieuwe studie vindt onnauwkeurigheden in arseentestkits in Bangladesh

- Vorming van goudbindingen in realtime gevolgd met behulp van nieuwe moleculaire spectroscopietechniek

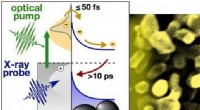
- Wetenschappers maken spontane snapshots van elektronen die licht oogsten op atomaire schaal
- Chemici maken playdough / Lego-achtige hybride om kleine bouwstenen te maken
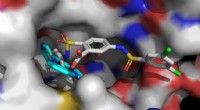
- Op weg naar de ontwikkeling van medicijnen voor aan veroudering gerelateerde ziekten
 NASA's Webb Sunshield ondergaat raketmontage, meer testen
NASA's Webb Sunshield ondergaat raketmontage, meer testen Faking-golven:hoe de NRA en pro-gun-Amerikanen de Australische misdaadstatistieken misbruiken
Faking-golven:hoe de NRA en pro-gun-Amerikanen de Australische misdaadstatistieken misbruiken  De definitie van lichaamssystemen
De definitie van lichaamssystemen Welk deeltje wordt uitgegeven wanneer fosfor-32 een transmutatiereactie ondergaat?
Welk deeltje wordt uitgegeven wanneer fosfor-32 een transmutatiereactie ondergaat?  Hoeveel oz in een fles van 375 ml?
Hoeveel oz in een fles van 375 ml?  Wanneer vindt een chemische reactie plaats?
Wanneer vindt een chemische reactie plaats?  Wat is de betekenis van fysieke hoeveelheden en metingen?
Wat is de betekenis van fysieke hoeveelheden en metingen?  Eigenschappen van broeikasgassen
Eigenschappen van broeikasgassen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


