
Wetenschap
Anionvorming begrijpen:waarom niet-metalen de neiging hebben elektronen te verkrijgen
Dit is waarom:
* Elektronegativiteit: Niet-metalen hebben een hogere elektronegativiteit dan metalen. Dit betekent dat ze een sterkere aantrekkingskracht hebben op elektronen.
* Elektronenconfiguratie: Niet-metalen hebben doorgaans bijna gevulde buitenste elektronenschillen. Door een of meer elektronen te verkrijgen, wordt hun schil compleet en worden ze stabieler.
Wanneer niet-metalen zich binden met metalen, verliezen de metaalatomen elektronen om kationen te worden (positief geladen ionen), en de niet-metalen krijgen die elektronen om anionen te worden (negatief geladen ionen). Dit resulteert in een ionische binding.
Voorbeelden van veel voorkomende anionen:
* Halogenen: Fluor (F-), Chloor (Cl-), Broom (Br-), Jodium (I-)
* Zuurstof: Oxide (O2-)
* Zwavel: Sulfide (S2-)
* Stikstof: Nitride (N3-)
Uitzonderingen:
Hoewel niet-metalen over het algemeen anionen vormen, zijn er enkele uitzonderingen. Waterstof kan in sommige verbindingen bijvoorbeeld een kation (H+) vormen.
 Nieuwe softwaretool extraheert belangrijke gegevens over blootstelling aan chemische stoffen
Nieuwe softwaretool extraheert belangrijke gegevens over blootstelling aan chemische stoffen Een robot en software maken het eenvoudiger om geavanceerde materialen te maken
Een robot en software maken het eenvoudiger om geavanceerde materialen te maken Wat is de gedolven verbinding van een metaal?
Wat is de gedolven verbinding van een metaal?  Chemicus synthetiseert nieuwe verbindingen met sterke antidiabetische eigenschappen
Chemicus synthetiseert nieuwe verbindingen met sterke antidiabetische eigenschappen Kan 1750 ml water oplossen 4.6 kopersulfaat CUSO4?
Kan 1750 ml water oplossen 4.6 kopersulfaat CUSO4?
 Sherpatekort eist zijn tol op Everest
Sherpatekort eist zijn tol op Everest De intensiteit van de trots die mensen voelen voor een bepaalde handeling of eigenschap wordt bepaald door een impliciete mentale kaart van wat anderen waarderen
De intensiteit van de trots die mensen voelen voor een bepaalde handeling of eigenschap wordt bepaald door een impliciete mentale kaart van wat anderen waarderen  Verborgen bedreiging voor de gezondheid
Verborgen bedreiging voor de gezondheid Betrokkenheid van lokale belanghebbenden essentieel voor inzicht in het beschermingsniveau van beschermde mariene gebieden
Betrokkenheid van lokale belanghebbenden essentieel voor inzicht in het beschermingsniveau van beschermde mariene gebieden Gelijktijdige hittegolven veroorzaakt door antropogene klimaatverandering
Gelijktijdige hittegolven veroorzaakt door antropogene klimaatverandering
Hoofdlijnen
- Is het evolutieproces waarmee de persoon die het beste zijn aangepast, overleven en zich voortplanten?
- Waarom enzymen zijn eiwitten?
- Welke voedingsmiddelen maken planten?
- Welke observatie bewijst dat een cel eukaryote is?
- Uit onderzoek blijkt wat ervoor zorgt dat plantenwortels sterk worden
- Wat is het meest voorkomende gedrag bij eenvoudige dieren zoals cnidarians en wormen?
- Welk organisme omringt hun prooi?
- Welke evolutionaire betekenis geven wetenschappers deze in groene algen?
- Wat is het beste of breedste niveau van het classificatiesysteem voor levende organismen die worden genoemd?
- Spectrometers uitgelegd:de samenstelling van materie ontsluiten met licht

- Nieuw onderzoek onthult de geheimen van fotosynthese die zouden kunnen helpen bij de ontwikkeling van computertechnologie

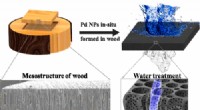
- Houtfilter verwijdert giftige kleurstof uit water
- Huidkankermysterie onthuld in yin- en yang-eiwit
- Kunnen we grafiet maken van steenkool? Onderzoekers beginnen met het vinden van nieuwe vaste koolstof

 Wat suggereert de theorie van plaattektoniek over het creëren van diepzee loopgraven?
Wat suggereert de theorie van plaattektoniek over het creëren van diepzee loopgraven?  Zeg je dat mechanische energie wordt geproduceerd in een speelgoedauto waarom?
Zeg je dat mechanische energie wordt geproduceerd in een speelgoedauto waarom?  Technologie voor het vervaardigen van nanodeeltjesclusters met behulp van DNA-bindend eiwit ontwikkeld
Technologie voor het vervaardigen van nanodeeltjesclusters met behulp van DNA-bindend eiwit ontwikkeld Welke lagen van de aarde bevatten rotsen?
Welke lagen van de aarde bevatten rotsen?  Waar zou men een plafondlamp kunnen kopen?
Waar zou men een plafondlamp kunnen kopen?  De activeringsenergie voor de chemische reactie in levende dingen is hoog of laag?
De activeringsenergie voor de chemische reactie in levende dingen is hoog of laag?  Hoe wordt de wrijving tussen de bewegende delen van een auto -motor verminderd?
Hoe wordt de wrijving tussen de bewegende delen van een auto -motor verminderd?  Onderzoekers vinden de uitstoot van nieuwe voertuigen bedrieglijk schoon
Onderzoekers vinden de uitstoot van nieuwe voertuigen bedrieglijk schoon
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

