
Wetenschap
Van der Waals-krachten:moleculaire aantrekkingskracht begrijpen
Er zijn drie soorten van der Waals-krachten:
* Verspreidingskrachten in Londen: Deze zijn het zwakste type en komen voor tussen alle moleculen, zelfs niet-polaire. Ze komen voort uit tijdelijke fluctuaties in de elektronenverdeling rond het molecuul.
* Dipool-dipoolkrachten: Deze komen voor tussen polaire moleculen die permanente dipolen hebben vanwege de ongelijke verdeling van elektronen.
* Waterstofbinding: Dit is het sterkste type van der Waals-kracht en treedt op wanneer een waterstofatoom is gebonden aan een zeer elektronegatief atoom (zoals zuurstof, stikstof of fluor).
Deze krachten zijn relatief zwak vergeleken met ionische of covalente bindingen, maar ze zijn nog steeds belangrijk bij het bepalen van de fysische eigenschappen van stoffen, zoals smeltpunt, kookpunt en oplosbaarheid.
 Wat zou hoogstwaarschijnlijk met een uiencel ervan gebeuren, in vloeistof met concentratie opgeloste stoffen worden geplaatst?
Wat zou hoogstwaarschijnlijk met een uiencel ervan gebeuren, in vloeistof met concentratie opgeloste stoffen worden geplaatst?  Wat is het symbool houtskool in periodieke tabel?
Wat is het symbool houtskool in periodieke tabel?  Wat is het verschil tussen een molecuul van zuurstof en methaan?
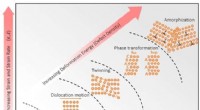
Wat is het verschil tussen een molecuul van zuurstof en methaan?  Onderzoekers gebruiken kunstmatige intelligentie om de geheimen van de anisotropie van magnesiumlegeringen te ontrafelen
Onderzoekers gebruiken kunstmatige intelligentie om de geheimen van de anisotropie van magnesiumlegeringen te ontrafelen  Wat is de meest zure pH 2 5 7 of 11?
Wat is de meest zure pH 2 5 7 of 11?
Hoofdlijnen
- Menselijke organen:een uitgebreide gids voor lichaamssystemen
- Namen van DNA-strengen
- Hoe verzamel en analyseer je bacteriën?
- Albuminen zijn de plasma-eiwitten die verantwoordelijk zijn voor?
- Welke soorten planten worden gebruikt om alcohol te maken?
- Het team vindt direct bewijs van rondtrekkende broedvogelsoorten aan de oostkust
- Welk bioom is eikenboom?
- Wanneer moeten wetenschappelijke modellen worden gewijzigd?
- leg uit waarom hormonen in de bloedbaan alleen doelcellen/organen kunnen beïnvloeden en niet andere cellen/organen?
- Hoe u de zuiverheid van stoffen kunt verifiëren:van visuele controles tot geavanceerde spectroscopie

- Nieuwe synthetische route voor amanitine, een therapeutisch interessant paddenstoelentoxine

- Hoe een chemische oplossing te concentreren door eenvoudige destillatie

- Eilanden zonder structuur in metaallegeringen kunnen leiden tot hardere materialen
- Buiten de kooi denken:een nieuwe benadering van energie-intensieve moleculaire scheidingen

 Wat zal veranderen als de lucht in een gesloten fles wordt verwarmd?
Wat zal veranderen als de lucht in een gesloten fles wordt verwarmd?  Van de plaats delict naar de rechtszaal - de reis van een DNA-monster
Van de plaats delict naar de rechtszaal - de reis van een DNA-monster Waarom belde Pluto meer een planeet?
Waarom belde Pluto meer een planeet?  Nieuw mechanisme van radio-emissie in neutronensterren vrijgegeven
Nieuw mechanisme van radio-emissie in neutronensterren vrijgegeven Tweetraps energiebeheersysteem verhoogt de efficiëntie van het oogsten van energie
Tweetraps energiebeheersysteem verhoogt de efficiëntie van het oogsten van energie Welk type stollingsgesteente wordt gevormd met uiteenlopende grenzen?
Welk type stollingsgesteente wordt gevormd met uiteenlopende grenzen?  Wetenschappers ontdekken dat vroege mensen eerder door Middellandse Zee trokken dan gedacht
Wetenschappers ontdekken dat vroege mensen eerder door Middellandse Zee trokken dan gedacht Schimmel nu geassocieerd met voedselkwaliteit
Schimmel nu geassocieerd met voedselkwaliteit
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

