
Wetenschap
Inzicht in de pH van ammoniakoplossingen:een uitgebreide gids
* Ammoniak in water: Wanneer ammoniak oplost in water, reageert het met watermoleculen om ammoniumionen (NH4+) en hydroxide-ionen (OH-) te vormen:
```
NH3 (water) + H2O (l) ⇌ NH4+ (water) + OH- (water)
```
* pH en hydroxide-ionen: De aanwezigheid van hydroxide-ionen (OH-) maakt de oplossing basisch. Hoe meer hydroxide-ionen, hoe hoger de pH.
* Concentratie is belangrijk: Hoe hoger de concentratie ammoniak, hoe meer hydroxide-ionen er worden geproduceerd en hoe hoger de pH.
Zo bepaal je de pH:
1. Bepaal de ammoniakconcentratie: U moet de molariteit (mol per liter) van de ammoniakoplossing kennen.
2. Gebruik de Kb-waarde: Ammoniak heeft een basisdissociatieconstante (Kb) van 1,8 x 10^-5. Deze waarde geeft aan hoeveel ammoniak in water ioniseert.
3. Bereken de hydroxide-ionenconcentratie: Aan de hand van de Kb-waarde en de ammoniakconcentratie bereken je de hydroxide-ionenconcentratie ([OH-]).
4. Bereken de pOH: pOH =-log[OH-]
5. Bereken de pH: pH + pOH =14
Voorbeeld:
Stel dat u een ammoniakoplossing van 0,1 M heeft. Met behulp van de Kb-waarde en enkele berekeningen kun je ontdekken dat de pH van deze oplossing ongeveer 11,1 is.
Belangrijke opmerkingen:
* De pH van ammoniakoplossingen kan variëren van licht basisch (ongeveer 8) voor zeer verdunde oplossingen tot sterk basisch (boven 11) voor meer geconcentreerde oplossingen.
* Als u met ammoniakoplossingen werkt, is het essentieel om er voorzichtig mee om te gaan, omdat ze irriterend kunnen zijn voor de huid en ogen.
 Welke structuren vormen het filtratiemembraan in Nephron?
Welke structuren vormen het filtratiemembraan in Nephron?  Een 2,14 g monster van natriumhypoiodiet wordt opgelost in water om 1,25 L oplossing te maken de pH 11.32 Welke KB voor ion?
Een 2,14 g monster van natriumhypoiodiet wordt opgelost in water om 1,25 L oplossing te maken de pH 11.32 Welke KB voor ion?  Hydroxylionen (OH⁻) begrijpen:eigenschappen en rol in basen
Hydroxylionen (OH⁻) begrijpen:eigenschappen en rol in basen  Hoe ziet hydrocholinezuur eruit?
Hoe ziet hydrocholinezuur eruit?  Waarom geeft een waterige oplossing van ammoniak een scherpe geur?
Waarom geeft een waterige oplossing van ammoniak een scherpe geur?
 Welk effect heeft geografie op het klimaat?
Welk effect heeft geografie op het klimaat?  In Noorwegen, flessen gemaakt van plastic zijn nog steeds fantastisch
In Noorwegen, flessen gemaakt van plastic zijn nog steeds fantastisch Seismologen:waarschuwingssystemen voor aardbevingen hebben een betere balans nodig tussen technische en voorspellende mogelijkheden
Seismologen:waarschuwingssystemen voor aardbevingen hebben een betere balans nodig tussen technische en voorspellende mogelijkheden Beheersen van de klimaatramp
Beheersen van de klimaatramp Wat is er aan de hand van levende materie?
Wat is er aan de hand van levende materie?
Hoofdlijnen
- Welk aminozuur zou worden geproduceerd als transcriptie plaatsvond van de DNA -sequentiekat?
- Wat is wanneer meer cellen worden gemaakt dan sterven?
- Wat doen wetenschappers na een onderzoek?
- Wie denk je dat echt is? De eerste genetische kaart op kleine schaal van de Britse eilanden
- Glycolyse: definitie, stappen, producten en reactanten
- Evolutie is een gok of serieuze theorie?
- Afrikaanse slaapziekte:hoe de ziekteverwekker tseetseevliegen koloniseert
- Wat is het proces waarmee wetenschapper elkaar controleert, werken vóór publicatie?
- Welk proces scheidt chromosomen?
- Onderzoek toont aan hoe kleine compartimenten aan cellen vooraf konden gaan

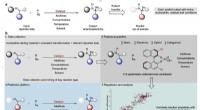
- De kans op succes in de synthetische chemie vergroten
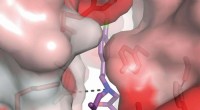
- Gericht op verborgen zak voor behandeling van beroerte en epileptische aanvallen
- Produceren van F-18-radiofarmaca voor PET-beeldvorming
- Nieuw platform voor het maken en karakteriseren van materiaalmengsels kan de ontwikkeling aanzienlijk versnellen

 Kunnen satellieten worden gebruikt als vroegtijdig waarschuwingssysteem voor aardverschuivingen?
Kunnen satellieten worden gebruikt als vroegtijdig waarschuwingssysteem voor aardverschuivingen?  Wat zijn de milieueffecten van mijnbouw en boren?
Wat zijn de milieueffecten van mijnbouw en boren?  Wat is een rots die mineralen bevat?
Wat is een rots die mineralen bevat?  Onderzoek naar genderongelijkheid toont aan dat vrouwen ondervertegenwoordigd zijn in wetenschappelijke tijdschriften op marketinggebied
Onderzoek naar genderongelijkheid toont aan dat vrouwen ondervertegenwoordigd zijn in wetenschappelijke tijdschriften op marketinggebied Hoe verandert de beweging en rangschikking van deeltjes als een substantie bevriest?
Hoe verandert de beweging en rangschikking van deeltjes als een substantie bevriest?  Hoe wordt elektriciteit verspild op scholen?
Hoe wordt elektriciteit verspild op scholen?  Nieuw onderzoek schetst hoe langere levens verband houden met fysieke activiteit
Nieuw onderzoek schetst hoe langere levens verband houden met fysieke activiteit  De afgestemde massademper:hoe de wetenschap de wolkenkrabbers van morgen aardbevingsbestendig kan maken
De afgestemde massademper:hoe de wetenschap de wolkenkrabbers van morgen aardbevingsbestendig kan maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

