
Wetenschap
Verschillen in covalente bindingen:chloor (Cl₂) versus zuurstof (O₂)
* Diatomisch chloor (Cl₂): Elk chlooratoom heeft 7 valentie-elektronen. Om een stabiel octet te bereiken, delen ze één paar elektronen (een enkele binding), waardoor Cl-Cl wordt gevormd.
* Diatomaire zuurstof (O₂): Elk zuurstofatoom heeft ook 6 valentie-elektronen. Om een stabiel octet te bereiken, delen ze twee elektronenparen (een dubbele binding), waardoor O=O ontstaat.
Hier is een samenvatting:
| Molecuul | Gedeelde elektronenparen | Obligatietype |
|---|---|---|
| Cl₂ | 1 | Enkele obligatie |
| O₂ | 2 | Dubbele binding |
Dit verschil in het aantal gedeelde elektronen leidt tot:
* Hechtsterkte: Dubbele bindingen zijn sterker dan enkele bindingen, wat betekent dat er meer energie nodig is om ze te verbreken.
* Lengte van de obligatie: Dubbele bindingen zijn korter dan enkele bindingen.
* Reactiviteit: Zuurstof is over het algemeen reactiever dan chloor vanwege de sterkere dubbele binding en hogere elektronegativiteit.
Daarom is het belangrijkste verschil in de covalente bindingen van diatomisch chloor en zuurstof het aantal gedeelde elektronenparen , resulterend in verschillende hechtsterkten, lengtes en reactiviteit.
 Wat gebeurt er als natriumcarbonaat wordt verwarmd?
Wat gebeurt er als natriumcarbonaat wordt verwarmd?  Is een ijsblokje een elementmengsel of verbinding?
Is een ijsblokje een elementmengsel of verbinding?  Wordt gemaakt van 2 of meer stoffen die samen in hetzelfde zijn, maar niet chemisch gecombineerd?
Wordt gemaakt van 2 of meer stoffen die samen in hetzelfde zijn, maar niet chemisch gecombineerd?  Welke materialen worden gebruikt om een bekeranemometer te maken?
Welke materialen worden gebruikt om een bekeranemometer te maken?  Wat zijn de producten die worden gevormd als een kaars wordt verbrand? Schrijf een passende reactievergelijking?
Wat zijn de producten die worden gevormd als een kaars wordt verbrand? Schrijf een passende reactievergelijking?
 Klimaatverandering zal de stroomstroming in het bovenste stroomgebied van de Colorado verminderen naarmate de grondwaterstanden dalen, zo blijkt uit onderzoek
Klimaatverandering zal de stroomstroming in het bovenste stroomgebied van de Colorado verminderen naarmate de grondwaterstanden dalen, zo blijkt uit onderzoek  VK verbiedt verkoop van benzine- en dieselauto's tegen 2040
VK verbiedt verkoop van benzine- en dieselauto's tegen 2040 Hoe stedelijke soundscapes mensen en dieren in het wild beïnvloeden, en wat er is veranderd in de stilte van de lockdown
Hoe stedelijke soundscapes mensen en dieren in het wild beïnvloeden, en wat er is veranderd in de stilte van de lockdown Studie:Noordwest hittegolf onmogelijk zonder klimaatverandering
Studie:Noordwest hittegolf onmogelijk zonder klimaatverandering Wat worden observaties die ze beschrijven?
Wat worden observaties die ze beschrijven?
Hoofdlijnen
- Wat is het eindproduct van fotosynthese?
- Wat is klier die de meeste spijsverteringsenzymen en enkele belangrijke hormonen afscheidt?
- Het doel van elektroforese
- Hoeveel sets van hetzelfde gen voor elk kenmerk ontvangen nakomelingen?
- Wetten van aantrekking:bestuivers gebruiken meerdere signalen om bloemen op verschillende continenten te identificeren
- Hoe ondersteunt biochemische overeenkomsten de evolutie?
- Wiens idee vormt de celtheorie?
- Wat vind je van het Human Genome Project?
- Kan e-learning de dreiging van invasieve uitheemse soorten zoals de Japanse duizendknoop helpen tegengaan?
- Snelle en efficiënte scheiding van olie en water bereikt door nieuw ontwikkelde deeltjes

- Een gepatenteerde oplossing voor het verlichten van droge mond en de ontwikkeling van voedingsproducten
- Hoe een citroenklok werkt:de wetenschap achter elektrolyse

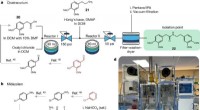
- Een computersysteem dat chemisch afval analyseert en manieren voorstelt om er nieuwe producten van te maken
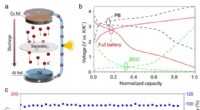
- Constructie van op koolstof gebaseerde celachtige bollen voor robuuste kaliumanode
 Hoe stroomt de elektriciteit van een krachtcentrale naar uw huis?
Hoe stroomt de elektriciteit van een krachtcentrale naar uw huis?  Google's uitdaging om gameconsoles in november van start te laten gaan
Google's uitdaging om gameconsoles in november van start te laten gaan De basale membraanlaag van de huid scheidt wat?
De basale membraanlaag van de huid scheidt wat?  Wetenschappers vinden gaten in licht door het in knopen te knopen
Wetenschappers vinden gaten in licht door het in knopen te knopen Waarom wordt het klimaat tropische marine genoemd?
Waarom wordt het klimaat tropische marine genoemd?  In welke reactie kan element en een verbinding meestal worden gecombineerd?
In welke reactie kan element en een verbinding meestal worden gecombineerd?  Laserbehandeling blijkt de prestaties van de batterij te verbeteren
Laserbehandeling blijkt de prestaties van de batterij te verbeteren  Nanodraad-arrays kunnen zonnecellen verbeteren
Nanodraad-arrays kunnen zonnecellen verbeteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

