Wetenschap
Hoe een citroenklok werkt:de wetenschap achter elektrolyse
Door Mallory Ferland
Bijgewerkt op 24 maart 2022
Hoe een citroenklok werkt
In de kern is een citroenklok een eenvoudige elektrochemische cel. Het zure sap in de vrucht werkt als een elektrolyt, waardoor ionen vrij kunnen bewegen. Wanneer twee ongelijksoortige metalen – meestal zink en koper – in de citroen worden geplaatst, dienen ze als elektroden. Elektronen stromen van het zink naar het koper via een externe draad, waardoor een kleine elektrische stroom ontstaat die een klok aandrijft.
Het elektrolyseproces uitgelegd
Elektrolyse is de beweging van elektrische stroom door een elektrolyt. In een citroenklok laat de zinkelektrode elektronen vrij, waardoor deze positief geladen wordt, terwijl de koperelektrode elektronen accepteert en negatief geladen wordt. De ionen in het citroensap migreren naar de tegengesteld geladen elektroden, voltooien het circuit en produceren de elektriciteitsstroom die nodig is om het mechanisme van de klok aan te drijven. Hoewel de energieopbrengst bescheiden is, is deze voldoende voor apparaten met een laag vermogen.
Commerciële citroenklokken
Veel commerciële modellen gebruiken kant-en-klare koper-zink pluggen die in een citroen klikken. Eenmaal ingebracht, brengt de plug de elektrochemische cel tot stand, en een verborgen draad verbindt de elektroden met de stroomingang van de klok. Deze klokken zijn vaak voorzien van analoge wijzerplaten en lopen enkele weken stil voordat de elektroden gaan corroderen.
DIY Citroenklokprojecten
Voor een demonstratie in het klaslokaal of een creatieve hobby kan met eenvoudige benodigdheden een zelfgemaakte citroenklok worden gebouwd. Rijg een reeks citroenen aan elkaar, prik ze elk met een speld of paperclip, wikkel de pinnen in aluminiumfolie en verbind ze met een koperdraad. Wanneer het circuit gesloten is, zal de elektrolytische reactie een kleine analoge of digitale klok van stroom voorzien. Zout water of andere zure oplossingen kunnen ook als elektrolyten dienen, wat alternatieve experimenten mogelijk maakt.
 Waarom is siliciumdioxide een vaste stof?
Waarom is siliciumdioxide een vaste stof?  Waarom is kwik een geschiktere vloeistof voor thermometer dan water en alcohol?
Waarom is kwik een geschiktere vloeistof voor thermometer dan water en alcohol?  Bevatten sterke bases meestal positief geladen atomen van hoge elektronegativiteit en geen resonantiestabilisatie?
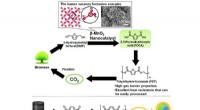
Bevatten sterke bases meestal positief geladen atomen van hoge elektronegativiteit en geen resonantiestabilisatie?  Nieuw leven vinden voor wijndruivenresten
Nieuw leven vinden voor wijndruivenresten U kunt zien of een mengsel oplossing of ophanging is wanneer u?
U kunt zien of een mengsel oplossing of ophanging is wanneer u?
 Mensen - de verontrustende buren van rifhaaien
Mensen - de verontrustende buren van rifhaaien Wat eet de harp zeehonden?
Wat eet de harp zeehonden?  Zealandia Switch is mogelijk de ontbrekende schakel in het begrijpen van ijstijdklimaten
Zealandia Switch is mogelijk de ontbrekende schakel in het begrijpen van ijstijdklimaten Wat groeien de planten in bladeren?
Wat groeien de planten in bladeren?  Verkeersdichtheid, wind- en luchtstratificatie beïnvloeden concentraties luchtverontreinigende stof stikstofdioxide
Verkeersdichtheid, wind- en luchtstratificatie beïnvloeden concentraties luchtverontreinigende stof stikstofdioxide
Hoofdlijnen
- Het eten voor dicot -embryo's wordt opgeslagen in de?
- Wat is de eerste stap in het decoderen van genetische berichten?
- Waarom is DNA van twee organismen van dezelfde soort polymorf?
- Studie beschrijft een algemene bacteriële verdediging tegen virale infecties
- Wat is de betekenis van de biologie van reproductieve klonen?
- Waar produceert fotosynthese voedsel voor?
- Welke genetische verandering is altijd een gevolg van evolutie?
- Doodt ontvetter of desinfectiemiddel bacteriën?
- Hoe kunnen nieuwe DNA -patronen in de natuur ontstaan?
 Bruikbare vormen van stikstof voor menselijke consumptie:een uitgebreide gids
Bruikbare vormen van stikstof voor menselijke consumptie:een uitgebreide gids  Wat is de juiste formule -vijand natriumion?
Wat is de juiste formule -vijand natriumion?  Waar worden zuurstof, silicium en aluminium in de aarde aangetroffen?
Waar worden zuurstof, silicium en aluminium in de aarde aangetroffen?  Vrijstaande fotoverknoopte eiwitpolymeerhydrogels voor langdurige afgifte van geneesmiddelen
Vrijstaande fotoverknoopte eiwitpolymeerhydrogels voor langdurige afgifte van geneesmiddelen Pas op, Mars:Hier komen we met een vloot ruimtevaartuigen
Pas op, Mars:Hier komen we met een vloot ruimtevaartuigen Welke verbindingen worden gevormd wanneer ijzer en zink reageren?
Welke verbindingen worden gevormd wanneer ijzer en zink reageren?  Welk volume van een 2,5 M voorraadoplossing azijnzuur (HC2H3O2) is nodig om te bereiden?
Welk volume van een 2,5 M voorraadoplossing azijnzuur (HC2H3O2) is nodig om te bereiden?  Vier redenen waarom het kwantumvacuüm donkere materie zou kunnen verklaren
Vier redenen waarom het kwantumvacuüm donkere materie zou kunnen verklaren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com