
Wetenschap
Wat zijn de producten die worden gevormd als een kaars wordt verbrand? Schrijf een passende reactievergelijking?
Verbrandingsreactie:
```
C25H52 + 38O2 → 25CO2 + 26H2O + energie (warmte en licht)
```
Bij deze reactie reageren de koolwaterstofmoleculen in het kaarsvet (C25H52) met zuurstof (O2) uit de omringende lucht, waarbij kooldioxide (CO2) en waterdamp (H2O) worden geproduceerd. De energie die vrijkomt bij deze verbrandingsreactie komt vrij in de vorm van warmte en licht, waardoor de kaars gaat branden en een vlam uitstraalt.
Pyrolysereactie:
Naast verbranding vindt bij het branden van kaarsen ook pyrolyse (de thermische ontleding van organisch materiaal bij afwezigheid van zuurstof) plaats. Dit proces leidt tot de vorming van verschillende tussenproducten en bijproducten, waaronder roet (koolstofdeeltjes), koolwaterstoffen en andere organische verbindingen. Deze bijproducten zijn verantwoordelijk voor de karakteristieke geur en uitstraling van kaarsvlammen.
De relatieve hoeveelheden CO2, H2O en roet die tijdens het branden van kaarsen worden geproduceerd, kunnen variëren afhankelijk van factoren zoals het gebruikte type was, de aanwezigheid van onzuiverheden en de brandomstandigheden. Kaarsen die zijn gemaakt met bepaalde wassoorten, zoals sojawas of bijenwas, hebben bijvoorbeeld de neiging minder roet te produceren in vergelijking met kaarsen van paraffinewas. Bovendien kunnen factoren zoals de grootte van de kaarsvlam, de beschikbaarheid van zuurstof en de luchtstromen in de omgeving het verbrandingsproces en de samenstelling van de gevormde producten beïnvloeden.
 Wetenschappers ontdekken nieuwe klasse van halfgeleidende entropie-gestabiliseerde materialen
Wetenschappers ontdekken nieuwe klasse van halfgeleidende entropie-gestabiliseerde materialen Chemische synthese met behulp van titaniumdioxide:een milieuvriendelijke en innovatieve aanpak
Chemische synthese met behulp van titaniumdioxide:een milieuvriendelijke en innovatieve aanpak  Polymeer gloeit omkeerbaar wit wanneer uitgerekt
Polymeer gloeit omkeerbaar wit wanneer uitgerekt Kan China de jaarlijkse vermindering van de vervuiling volhouden?
Kan China de jaarlijkse vermindering van de vervuiling volhouden?  Hoe goed bevatten natte maskers druppels? Onderzoek toont aan dat vocht de penetratie van ademhalingsdruppels nog steeds verhindert
Hoe goed bevatten natte maskers druppels? Onderzoek toont aan dat vocht de penetratie van ademhalingsdruppels nog steeds verhindert
 NASA vindt windschering verzwakking van tropische storm Nadine
NASA vindt windschering verzwakking van tropische storm Nadine Antarctische ijsscheur nabij afkalven, na een groei van 17 km in 6 dagen
Antarctische ijsscheur nabij afkalven, na een groei van 17 km in 6 dagen De dieptepunten en dieptepunten van het Antarctische zee-ijs
De dieptepunten en dieptepunten van het Antarctische zee-ijs  Verschillende hydraulische systemen
Verschillende hydraulische systemen  Europa wankelt van de ergste overstromingen in jaren terwijl het dodental 120 . overschrijdt
Europa wankelt van de ergste overstromingen in jaren terwijl het dodental 120 . overschrijdt
Hoofdlijnen
- Soorten organismen die van plantencellen zijn gemaakt
- Wat kan er gebeuren als Meiose verkeerd gaat?
- Onderzoek naar de rol van methylering bij vernalisatie en fotoperiode-route:een potentiële bloeiregulator?
- Coyotes in New York City hoeven niet afhankelijk te zijn van menselijke voeding
- Hoe een vis kan braden:wetenschappers ontdekken evolutionaire aanwijzingen achter elektriciteit
- Hoe een tRNA-reeks te krijgen van een DNA-reeks
- Welke soorten plantencellen zijn er?
- Was de grote omvang van de sauropode dinosaurussen te danken aan plantaardig voedsel? Wetenschappers beweren dat het oude idee nog steeds benen heeft
- Welke cel heeft een gebrek aan membraangebonden kern?
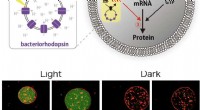
- Wetenschapper bouwt kunstmatige fotosynthetische cellen
- Extreme UV-laser toont de vorming van luchtverontreinigende stoffen

- Vastestofkatalyse:fluctuaties maken de weg vrij

- Poreus kristal leidt reactie om koolstofdioxide te transformeren

- Wetenschappers ontwikkelen moleculaire code voor melanine-achtige materialen

 Borophene gaat vooruit als platform voor 2D-materialen
Borophene gaat vooruit als platform voor 2D-materialen Onderzoekers passen voor het eerst 2D-spectroscopie toe op geïsoleerde moleculaire systemen
Onderzoekers passen voor het eerst 2D-spectroscopie toe op geïsoleerde moleculaire systemen Thuiswerken kan je gelukkiger maken, vooral als je getrouwd bent
Thuiswerken kan je gelukkiger maken, vooral als je getrouwd bent Hoe nematoden de verdediging van ongedierte te slim af zijn
Hoe nematoden de verdediging van ongedierte te slim af zijn  Waarom volle dammen geen waterveiligheid betekenen:een blik op Zuid-Afrika
Waarom volle dammen geen waterveiligheid betekenen:een blik op Zuid-Afrika Wind, warm water wakkerde smeltende Antarctische gletsjers aan
Wind, warm water wakkerde smeltende Antarctische gletsjers aan Vulkanische as kan helpen bij het verminderen van koolstofdioxide in verband met klimaatverandering
Vulkanische as kan helpen bij het verminderen van koolstofdioxide in verband met klimaatverandering Hoe de lichtintensiteit te berekenen
Hoe de lichtintensiteit te berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

