
Wetenschap
Koolstof en silicium:4 valentie-elektronen voor binding begrijpen
Dit is waarom:
* Koolstof: Koolstof heeft atoomnummer 6, wat betekent dat het 6 elektronen heeft. De elektronenconfiguratie is 1s²2s²2p². Hierdoor krijgt het 4 valentie-elektronen (de elektronen in de buitenste schil) die beschikbaar zijn voor binding.
* Silicium: Silicium heeft een atoomnummer van 14, met een elektronenconfiguratie van 1s²2s²2p⁶3s²3p². Het heeft ook 4 valentie-elektronen in de buitenste schil.
Zowel koolstof als silicium bevinden zich in Groep 14 (IVA) van het periodiek systeem, en ze staan bekend om hun vermogen om vier covalente bindingen te vormen vanwege het feit dat ze vier valentie-elektronen hebben. Deze eigenschap is van fundamenteel belang voor hun rol in de organische chemie en de vorming van veel anorganische verbindingen.
 Wat voor soort atoomreactie vindt plaats op de zon?
Wat voor soort atoomreactie vindt plaats op de zon?  Bevriest water om een ijschemische verandering te vormen?
Bevriest water om een ijschemische verandering te vormen?  Experimenten en analyses laten zien hoe elektronen en protonen samenkomen op een elektrodeoppervlak
Experimenten en analyses laten zien hoe elektronen en protonen samenkomen op een elektrodeoppervlak Recente vorderingen in de optimalisatie van gedispergeerde platinakatalysatoren
Recente vorderingen in de optimalisatie van gedispergeerde platinakatalysatoren Welke van deze zouten smelt ijs sneller gewone tafel Saltkosher zout epsom en rots?
Welke van deze zouten smelt ijs sneller gewone tafel Saltkosher zout epsom en rots?
Hoofdlijnen
- Wat voor soort reactie is cellulaire ademhaling?
- Wilde dieren vormen grote bedreiging voor Outback, klimaatverandering studie vindt
- Wat is de classificatie van schimmels?
- Een klein niet -levend deeltje dat binnenkomt en de reproduceert in een levende cel?
- Verlies en hoop:Amerikaanse parkwachters bestrijden de klimaatcrisis
- Vertonen alle bacteriën een vergelijkbaar cultureel kenmerk?
- Wat wordt gevormd wanneer bemesting optreedt?
- DNA als boek:het ontsluiten van de geheimen van genetische informatie
- Een verenigend concept dat de basis vormt van wetenschappelijk onderzoek in een bepaald gebied wordt een genoemd?
- Durian skin-biocomposiet voor afhaalcontainers en 3D-printen

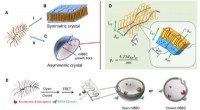
- De kristalsymmetrie van de natuur onderbreken om gerichte medicijnafgifte te bevorderen
- Onderzoekers demonstreren een fundamenteel nieuwe benadering van echografie

- Water helpt bij de onverwachte en ultrasnelle synthese van collageenachtig synthetisch poly-L-proline

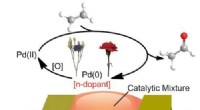
- Ethyleensensor kan helpen bij het bewaken van de gezondheid van planten
 Natriumbromide opgelost in watervergelijking?
Natriumbromide opgelost in watervergelijking?  Wat u moet weten over de totale zonsverduistering van volgende week in de VS, Mexico en Canada
Wat u moet weten over de totale zonsverduistering van volgende week in de VS, Mexico en Canada  Microplastics in garnalen onschadelijk voor diergezondheid en geen effecten op consumptiekwaliteit
Microplastics in garnalen onschadelijk voor diergezondheid en geen effecten op consumptiekwaliteit Hoe kan de gevoeligheid van een thermometer worden vergroot?
Hoe kan de gevoeligheid van een thermometer worden vergroot?  Een gratis manier om de resolutie van neutronenverstrooiing met 500% te verbeteren
Een gratis manier om de resolutie van neutronenverstrooiing met 500% te verbeteren Deadline sluiting voor namen om op NASA's volgende Marsrover te vliegen
Deadline sluiting voor namen om op NASA's volgende Marsrover te vliegen Wat is dat extra in mijn online winkelwagen? Binnenkort misschien een omzetbelasting
Wat is dat extra in mijn online winkelwagen? Binnenkort misschien een omzetbelasting  Wat is een andere naam voor de tweede bewegingswet?
Wat is een andere naam voor de tweede bewegingswet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

