
Wetenschap
Inzicht in de ionische aard van lithiumjodide (LiI)
* Verschil in elektronegativiteit: Lithium (Li) heeft een elektronegativiteit van 0,98, terwijl jodium (I) een elektronegativiteit van 2,66 heeft. Dit grote verschil in elektronegativiteit (1,68) geeft aan dat elektronen sterk naar het jodiumatoom worden getrokken.
* Ionische binding: Door deze elektronenoverdracht verliest lithium een elektron om een positief geladen lithiumion (Li+) te worden, terwijl jodium een elektron krijgt om een negatief geladen jodide-ion (I-) te worden. Deze tegengesteld geladen ionen trekken elkaar aan en vormen een ionische binding.
* Eigenschappen: Ionische verbindingen hebben doorgaans hoge smelt- en kookpunten, zijn oplosbaar in polaire oplosmiddelen zoals water en geleiden elektriciteit wanneer ze gesmolten of opgelost zijn. Deze eigenschappen zijn kenmerkend voor lithiumjodide.
Covalente verbindingen worden gevormd wanneer atomen elektronen delen, wat leidt tot een gelijkmatigere verdeling van de elektronendichtheid. Hoewel sommige ionische verbindingen een lichte mate van covalent karakter kunnen hebben, wordt LiI in de eerste plaats als ionisch beschouwd vanwege het aanzienlijke verschil in elektronegativiteit en de algehele ionische aard van zijn eigenschappen.
Hoofdlijnen
- Hoe natuurlijke selectie werkt
- Wat doet Mitchondria in een cel?
- Welke term verwijst naar de biologische dimensie van een mannelijk of vrouwelijk mens?
- Hoe verschilt differentiatie van vastberadenheid?
- Waar bevinden zich de 6 biomen?
- Produceert een hormoon dat het metabolisme reguleert?
- Wat regelt welke stoffen een cel binnenkomen en verlaten?
- Waarom zijn het allemaal levende wezens afkomstig van een gewone of universele voorouder?
- Zijn mutaties nuttig of schadelijk voor een organisme?
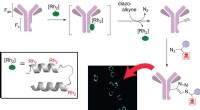
- Metaal vereenvoudigt de synthese van antilichaamgeneesmiddelen
- Polymeren raken verstrikt in haat-liefde chemie tussen olie en water

- Anionen en kationen in dual-ionbatterijen werken als koeherders- en weversmeisjes

- Hoe u de uiteindelijke concentratie kunt berekenen bij het mengen van oplossingen met verschillende sterktes

- Onderzoek naar de dynamiek van de vorming van nanodeeltjes uit een voorloper met atomaire resolutie

 Kleine elektrische velden kunnen een beslissende rol spelen bij de vorming van diamant
Kleine elektrische velden kunnen een beslissende rol spelen bij de vorming van diamant Welke ruimte -ambachten hebben Neptunus waargenomen?
Welke ruimte -ambachten hebben Neptunus waargenomen?  Generaliseren vliegen herinneringen net als mensen met PTSS?
Generaliseren vliegen herinneringen net als mensen met PTSS?  Wat is de naam en het aantal atomen elk element in samengestelde periodieke tabel NaCl H2O2 Fe3O4 SiO2?
Wat is de naam en het aantal atomen elk element in samengestelde periodieke tabel NaCl H2O2 Fe3O4 SiO2?  Hoeveel atomen zijn er in 2 mol hij?
Hoeveel atomen zijn er in 2 mol hij?  Trillen atomen minder als ze heter zijn?
Trillen atomen minder als ze heter zijn?  Geo-engineering polaire gletsjers om zeespiegelstijging te vertragen
Geo-engineering polaire gletsjers om zeespiegelstijging te vertragen De oorzaken van overstromingen
De oorzaken van overstromingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


