
Wetenschap
Zuurstof versus waterstof:elektronegativiteit en polariteit begrijpen
Dit is waarom:
* Elektronegativiteit: Zuurstof is elektronegatiever dan waterstof. Elektronegativiteit is het vermogen van een atoom om elektronen naar zich toe te trekken in een chemische binding.
* Elektronen delen: In de H-O-binding trekt zuurstof de gedeelde elektronen sterker aan dan waterstof. Dit betekent dat de elektronen meer tijd rond het zuurstofatoom doorbrengen.
* Gedeeltelijke kosten: Als resultaat van deze ongelijke elektronendeling ontwikkelt zuurstof een gedeeltelijk negatieve lading (δ-) en ontwikkelt waterstof een gedeeltelijk positieve lading (δ+).
Deze ongelijke verdeling van de lading creëert een polaire covalente binding in het watermolecuul.
 Een vorm van zuurstof met een scherpe oder?
Een vorm van zuurstof met een scherpe oder?  Onderzoekers voorspellen falen in ongeordende materialen
Onderzoekers voorspellen falen in ongeordende materialen Waarom smolt je ijsblokje sneller in water dan zoete thee -spritmelk appelsap en cola op 70 graden?
Waarom smolt je ijsblokje sneller in water dan zoete thee -spritmelk appelsap en cola op 70 graden?  Zit butaan in groep 2 van het periodiek systeem?
Zit butaan in groep 2 van het periodiek systeem?  Wat de hypothese van het splitsen van het waterwetenschappelijk project?
Wat de hypothese van het splitsen van het waterwetenschappelijk project?
 De ecologische voetafdruk van het avondeten:hoe 'groen' zijn vissticks?
De ecologische voetafdruk van het avondeten:hoe 'groen' zijn vissticks?  80 jaar sinds de eerste berekeningen aantoonden dat de aarde opwarmde door de toenemende uitstoot van broeikasgassen
80 jaar sinds de eerste berekeningen aantoonden dat de aarde opwarmde door de toenemende uitstoot van broeikasgassen Wat moet u overwegen om een complex milieuprobleem volledig te begrijpen?
Wat moet u overwegen om een complex milieuprobleem volledig te begrijpen?  De natuurlijke koolstofputten van de aarde hebben een vitale kracht in de strijd tegen het klimaat
De natuurlijke koolstofputten van de aarde hebben een vitale kracht in de strijd tegen het klimaat Hoe de opwarming van de aarde te beperken tot 1,5°C
Hoe de opwarming van de aarde te beperken tot 1,5°C
Hoofdlijnen
- leeuwen, chimpansees, haaien krijgen extra bescherming onder VN-verdrag
- DNA-transcriptie: hoe werkt het?
- Lijst ten minste vijf biologit van eenentwintigste Cuntury Ant Hun belangrijke bijdragen aan de biotechnologie?
- Waar bevindt zich het grootste deel van het DNA in een eukaryotische cel?
- Wat is de betekenis van waterorganisme?
- Welke mogelijke effecten kan een mutatie hebben op een organisme?
- Hoe heet het wanneer DNA veranderde of veranderd?
- Waar staat NUC voor in een cel?
- Biologische vergroting:inzicht in biomagnificatie in voedselketens
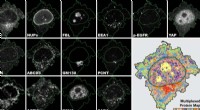
- Nieuwe methode verfijnt analyse van celmonsters
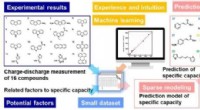
- Beste prestaties van organisch materiaal voor lithiumbatterijanode met behulp van materiaalinformatica
- VTT ontwikkelt transparante cellulosefilm ter vervanging van traditioneel plastic in voedselverpakkingen

- Schadeproductie en stralingsvermenging in materialen heroverwegen

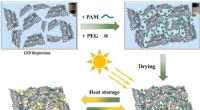
- Onderzoekers stellen een eenstapsstrategie voor om op grafeen gebaseerde composietfaseveranderingsmaterialen te synthetiseren
 Wat wordt er gevormd uit elementen?
Wat wordt er gevormd uit elementen?  Waarom zou een wetenschapper zijn hypothese heroverwegen?
Waarom zou een wetenschapper zijn hypothese heroverwegen?  Gebruik van smeltpolymerisatie om robuust covalent organisch raamwerkschuim te fabriceren
Gebruik van smeltpolymerisatie om robuust covalent organisch raamwerkschuim te fabriceren Chemici testen een nieuwe nanokatalysator voor het verkrijgen van waterstof
Chemici testen een nieuwe nanokatalysator voor het verkrijgen van waterstof Wat is de beweging van thermische energie van een warmer object naar koeler genoemd?
Wat is de beweging van thermische energie van een warmer object naar koeler genoemd?  Hoe een hekel aan lessen het vreemdgaan van studenten beïnvloedt
Hoe een hekel aan lessen het vreemdgaan van studenten beïnvloedt Wat gebeurt er als gebalanceerde krachten op een object handelen?
Wat gebeurt er als gebalanceerde krachten op een object handelen?  Waar gaat de maan heen als de zon in de lucht is?
Waar gaat de maan heen als de zon in de lucht is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

