
Wetenschap
De unieke reactiviteit van fluor:waarom het reageert met xenon, niet met jodium
1. Elektronegativiteit en ionisatie-energie:
* Fluor: Fluor is het meest elektronegatieve element, wat betekent dat het een sterke neiging heeft om elektronen aan te trekken. Het heeft ook een zeer hoge ionisatie-energie, wat betekent dat het moeilijk is om een elektron uit een fluoratoom te verwijderen.
* Xenon: Xenon is een edelgas en heeft een relatief lage ionisatie-energie, waardoor het gemakkelijker wordt om een elektron uit een xenonatoom te verwijderen.
2. Het fluoreffect:
* Fluor is ongelooflijk reactief vanwege de hoge elektronegativiteit en het kleine formaat. Het kan de edelgasconfiguratie van xenon overwinnen en een binding vormen. Dit staat bekend als het ‘fluoreffect’.
3. Jodium versus fluor:
* Jodium: Hoewel jodium ook een halogeen is, is het veel minder elektronegatief dan fluor. Het heeft ook een grotere atoomstraal, wat betekent dat de buitenste elektronen verder van de kern verwijderd zijn en minder stevig vastgehouden worden.
* Gebrek aan reactiviteit: Jodium mist de noodzakelijke elektronegativiteit en heeft niet het "fluoreffect" om de stabiele elektronische configuratie van xenon te overwinnen.
Samengevat: Het belangrijkste verschil ligt in de relatieve elektronegativiteit en ionisatie-energieën van de betrokken elementen. De buitengewone reactiviteit van fluor en het vermogen om de edelgasconfiguratie te overwinnen, zorgen ervoor dat het kan reageren met xenon, terwijl jodium deze eigenschappen mist.
 Verbindingen met het grootste ionische karakter zouden zich vormen als fluor reageert met?
Verbindingen met het grootste ionische karakter zouden zich vormen als fluor reageert met?  Is kookpunt een fysische of chemische eigenschap?
Is kookpunt een fysische of chemische eigenschap?  Hoeveel ionen worden er gemaakt als natriumsulfaat oplost in water?
Hoeveel ionen worden er gemaakt als natriumsulfaat oplost in water?  Ionengeleidend polymeer cruciaal voor het verbeteren van neuromorfe apparaten
Ionengeleidend polymeer cruciaal voor het verbeteren van neuromorfe apparaten Kan fosfor in de atmosfeer worden aangetroffen?
Kan fosfor in de atmosfeer worden aangetroffen?
Hoofdlijnen
- Welke lichaamssystemen werken samen om de vanaf ziekteverwekkers te beschermen?
- Giststudies tonen aan dat voeding in het vroege leven een positieve invloed kan hebben op de levenslange gezondheid
- Hoe promoters genen aanzetten:de sleutel tot DNA-transcriptie
- Wat is de wetenschappelijke naam voor flagellated protozoa?
- Hoe werken het ademhalingsstelsel en het cardiovasculaire systeem samen?
- Organismen of vloeistoffen die proberen het cellichaam van een neuron te betreden, moeten eerst door de?
- Wat is de algemene term voor alle cellulaire inhoud tussen plasmamembraan en kern?
- Cultureel liften:hoe sociaal gedrag de genetische samenstelling van dolfijnen kan beïnvloeden
- Wat voor soort weefsel is kalkoenvlees?
- Onderzoekers voltooien fase één menselijke proeven met slimme pillen

- Onderzoekers geven eerste chemische kaart van kleurstoffen vrij uit historische kleurstofbibliotheek

- Manipuleren van liganden:een nieuwe dimensie voor het bevorderen van elektrokatalyseprestaties door aerogels van edelmetaal
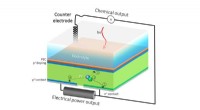
- Een zonnecel die dubbel werk doet voor hernieuwbare energie
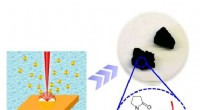
- Een lasergestuurde programmeerbare contactloze transferdruktechniek

 Welke twee factoren hangt de warmtecapaciteit van een object af?
Welke twee factoren hangt de warmtecapaciteit van een object af?  Hoe stabiel zijn arseenverbindingen in eetbare algen?
Hoe stabiel zijn arseenverbindingen in eetbare algen?  Misvattingen over klimaatverandering die veel voorkomen bij leraren, studie vondsten
Misvattingen over klimaatverandering die veel voorkomen bij leraren, studie vondsten Orkanen Irma en Maria hebben tijdelijk de koren van land- en zeedieren veranderd
Orkanen Irma en Maria hebben tijdelijk de koren van land- en zeedieren veranderd Benzinestations laten veel meer giftige dampen ontsnappen dan eerder werd gedacht
Benzinestations laten veel meer giftige dampen ontsnappen dan eerder werd gedacht Wie is de vader van de moderne biotechnologie?
Wie is de vader van de moderne biotechnologie?  Skelet- en endocriene systemen:hoe ze samenwerken
Skelet- en endocriene systemen:hoe ze samenwerken  Huawei getroffen door Amerikaanse exportcontroles, mogelijk importverbod
Huawei getroffen door Amerikaanse exportcontroles, mogelijk importverbod
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

