
Wetenschap
Ionische oplossing begrijpen:waarom zouten oplossen in water
1. Polariteit en aantrekkingskracht
* Water is een polair molecuul: Het zuurstofatoom in water heeft een licht negatieve lading, terwijl de waterstofatomen een licht positieve lading hebben. Hierdoor ontstaat een dipoolmoment.
* Ionische verbindingen zijn gemaakt van ionen: Ze bestaan uit positief geladen kationen en negatief geladen anionen die bij elkaar worden gehouden door elektrostatische krachten.
* Aantrekking tussen water en ionen: De positieve uiteinden van watermoleculen (waterstofatomen) worden aangetrokken door de negatief geladen anionen in de ionische verbinding. Op dezelfde manier worden de negatieve uiteinden van watermoleculen (zuurstofatomen) aangetrokken door de positief geladen kationen.
2. Het ontbindingsproces
1. Hydratatie: Wanneer een ionische verbinding in water wordt geplaatst, omringen watermoleculen de ionen en vormen ze hydratatieschillen. De aantrekkingskrachten tussen de watermoleculen en de ionen zijn sterker dan de krachten die de ionen in het kristalrooster bij elkaar houden.
2. Scheiding: De aantrekkingskracht tussen de watermoleculen en de ionen overwint de ionische bindingen die de verbinding bij elkaar houden, waardoor de ionen zich scheiden en door het water verspreiden.
3. Ontbinding: Het resultaat is de vorming van een oplossing waarbij de ionen worden omgeven door watermoleculen, waardoor de ionische verbinding effectief wordt opgelost.
3. Factoren die de oplosbaarheid beïnvloeden
* Ladingsdichtheid: Ionen met een hogere ladingsdichtheid (grotere lading in een kleiner volume) hebben een sterkere aantrekkingskracht op watermoleculen, wat leidt tot een grotere oplosbaarheid.
* Roosterenergie: De sterkte van de ionische bindingen in het kristalrooster beïnvloedt de oplosbaarheid. Verbindingen met zwakkere roosterenergie zullen eerder oplossen.
* Temperatuur: De oplosbaarheid van de meeste ionische verbindingen neemt toe met de temperatuur, omdat de verhoogde kinetische energie helpt de aantrekkingskracht tussen ionen in de vaste stof te overwinnen.
Samengevat: Ionische verbindingen lossen op in water omdat de sterke aantrekkingskracht tussen watermoleculen en de ionen de elektrostatische krachten overwint die de ionen bij elkaar houden in het kristalrooster. Dit proces omvat de vorming van hydratatieschillen rond de ionen en de daaropvolgende scheiding en verspreiding van ionen in het water.
 Onderzoekers onderzoeken de oppervlakte-extractie van platinakatalysatoren in alkalische media
Onderzoekers onderzoeken de oppervlakte-extractie van platinakatalysatoren in alkalische media  Als suiker wordt opgelost in water, welke component zal de opgeloste stof en oplosmiddel zijn?
Als suiker wordt opgelost in water, welke component zal de opgeloste stof en oplosmiddel zijn?  Vormen slechts twee gassen zure regen?
Vormen slechts twee gassen zure regen?  Welk edelgas zou hoogstwaarschijnlijk een verbinding vormen met fluor?
Welk edelgas zou hoogstwaarschijnlijk een verbinding vormen met fluor?  Evaluatie van nieuwe verwerkingsplatforms voor farmaceutische productie
Evaluatie van nieuwe verwerkingsplatforms voor farmaceutische productie
 Waarom wordt gematigd bos laadachtig bos genoemd?
Waarom wordt gematigd bos laadachtig bos genoemd?  NASA krijgt een infrarood babyfoto van de tropische storm Kristy
NASA krijgt een infrarood babyfoto van de tropische storm Kristy Bliksemafleiders gebruiken op een strand om glas te maken
Bliksemafleiders gebruiken op een strand om glas te maken Hoe Neanderthalers zich aanpasten aan de klimaatverandering
Hoe Neanderthalers zich aanpasten aan de klimaatverandering  Onderwijs beïnvloedt de religiositeit van Amerikanen – maar niet hoe je zou denken
Onderwijs beïnvloedt de religiositeit van Amerikanen – maar niet hoe je zou denken
Hoofdlijnen
- Cellulaire ademhaling vindt plaats in de van een cel?
- Nieuw onderzoek geeft aan hoe deep learning gentherapieën en antivirale medicijnen kan verbeteren
- Wat is munificatie in biotechnologie?
- 7 soorten bindweefsel
- Kikkervisjes voor het avondeten? Inheemse gemeenschap in Mexico onthult een favoriet recept voor een bepaalde kikker
- Wat is de functie van anastomoses?
- Evolutie en ecologische concurrentie van meercellige levenscycli
- Wat is de gemeenschappelijke naam voor Thermus Aquaticus?
- Wat is biotictechnologie?
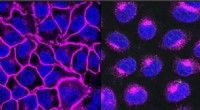
- Chemici maken moleculaire scalpels om ongewenste eiwitten van celoppervlakken te verwijderen
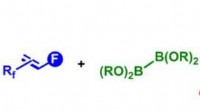
- Chemici ontsluiten het potentieel van fluoralkenen
- Geïdentificeerd:Moleculaire structuur die een belangrijk onderdeel van smog afbreekt

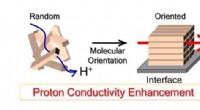
- Meer controle krijgen over brandstofcelmembranen
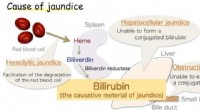
- Onderzoekers maken doorbraak in antioxidant-enzym gekoppeld aan geelzucht
 World Wetlands Day:wereldwijde biodiversiteit bevorderen en klimaatverandering tegengaan
World Wetlands Day:wereldwijde biodiversiteit bevorderen en klimaatverandering tegengaan Helpers bij het nest kunnen moedervogels toestaan kleinere eieren te leggen
Helpers bij het nest kunnen moedervogels toestaan kleinere eieren te leggen Techniek lokaliseert robots, soldaten in gebieden met GPS-problemen
Techniek lokaliseert robots, soldaten in gebieden met GPS-problemen Welke kleigrond bevat?
Welke kleigrond bevat?  Wat zijn de drie soorten diffusie?
Wat zijn de drie soorten diffusie?  Hoe is kinetische bewegingssenergie gerelateerd aan een vloeistofsolidgas en plasma?
Hoe is kinetische bewegingssenergie gerelateerd aan een vloeistofsolidgas en plasma?  Kunnen open en eerlijke wetenschappers het vertrouwen van het publiek winnen?
Kunnen open en eerlijke wetenschappers het vertrouwen van het publiek winnen?  Doet een zeer efficiënte machine relatief hoog of laag percentage energie af aan thermische energie?
Doet een zeer efficiënte machine relatief hoog of laag percentage energie af aan thermische energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

