
Wetenschap
Fluoratoomstraal:vergelijking met zuurstof en chloor
* Fluor (F): De kleinste atoomstraal van de drie.
* Zuurstof (O): Groter dan fluor, maar kleiner dan chloor.
* Chloor (Cl): De grootste atoomstraal van de drie.
Waarom is dit?
* Periodieke trends: De atoomstraal neemt over het algemeen toe naarmate u een groep (kolom) naar beneden beweegt in het periodiek systeem, en neemt af naarmate u van links naar rechts over een periode (rij) beweegt.
* Elektronegativiteit: Fluor is het meest elektronegatieve element, wat betekent dat het sterk elektronen aantrekt. Deze sterke aantrekkingskracht maakt de elektronenwolk compacter, wat resulteert in een kleinere atoomstraal.
* Afscherming: Naarmate je een groep lager gaat, neemt het aantal elektronenschillen toe, waardoor er meer afscherming ontstaat tussen de kern en de buitenste elektronen. Dit vermindert de effectieve nucleaire lading en vergroot de atomaire straal.
Samengevat:
De kleine atoomstraal van fluor is te danken aan de hoge elektronegativiteit en het feit dat het slechts twee elektronenschillen heeft. Zuurstof heeft een grotere straal vanwege de iets lagere elektronegativiteit en een extra elektronenschil. Chloor heeft de grootste straal omdat het nog meer elektronenschillen heeft, waardoor een grotere afscherming ontstaat en de effectieve nucleaire lading wordt verminderd.
Hoofdlijnen
- Vrouwelijke wetenschappers die de wereld veranderden
- Groot-Brittannië kondigt plan aan om handel in antiek ivoor te verbieden
- Designerpeptiden tonen potentieel voor het blokkeren van virussen en moedigen toekomstig onderzoek aan
- Hoe reguleert Ph de ademhaling?
- Bestaat er een verband tussen intelligentie en psychische aandoeningen?
- Wat zijn hormonen waar ze produceerden en hoe getransporteerd?
- Wetenschapper hebben genen in rijstplanten ingevoegd?
- Wat is de homofoon voor genen?
- Ondanks frequente waarnemingen zijn de leefgebieden van rode eekhoorns in Berlijn klein en gefragmenteerd
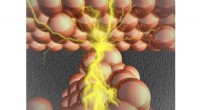
- De kloof op nanoschaal overbruggen:een diepe blik in atomaire schakelaars
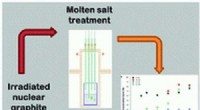
- Nieuwe behandelingstechnologie kan de belasting van nucleair afval in het VK verminderen
- Ingenieurs gebruiken Tiki-fakkels bij onderzoek naar roet, dieselfilters

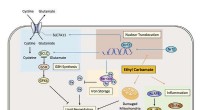
- Wetenschappers ontdekken het mechanisme voor ethylcarbamaat-geïnduceerde toxiciteit in gefermenteerd voedsel
- Er komt iets slecht (ruikend) op deze manier - de wetenschap van stoffen en geuren

 Kun je bladeren en stengels op anijsplanten eten?
Kun je bladeren en stengels op anijsplanten eten?  Verandert de snelheid van een object wanneer snelheid verandert?
Verandert de snelheid van een object wanneer snelheid verandert?  Hoe teken je een wereldkaart?
Hoe teken je een wereldkaart?  Wat drijft consumenten werkelijk om zich aan te melden voor door de gemeenschap ondersteunde landbouw?
Wat drijft consumenten werkelijk om zich aan te melden voor door de gemeenschap ondersteunde landbouw?  De meeste steden in Californië weigeren zich terug te trekken uit de stijgende zeeën; één stad wil laten zien hoe het moet
De meeste steden in Californië weigeren zich terug te trekken uit de stijgende zeeën; één stad wil laten zien hoe het moet  Wat zijn vijf fysieke eigenschappen van chloor?
Wat zijn vijf fysieke eigenschappen van chloor?  Draadtap op het dak is bedoeld om te leren waar kraaien over roddelen in de schemering
Draadtap op het dak is bedoeld om te leren waar kraaien over roddelen in de schemering Wat heeft Microsoft nodig in zijn volgende CEO?
Wat heeft Microsoft nodig in zijn volgende CEO?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


