
Wetenschap
Salpeterzuur versus zwavelzuur:de zuurgraad begrijpen
Dit is waarom:
* Sterkte van het zuur: De zuurgraad wordt bepaald door het vermogen van een zuur om protonen (H+-ionen) te doneren. Zwavelzuur is een sterker zuur omdat het gemakkelijk beide protonen afstaat, terwijl salpeterzuur er slechts één afstaat.
* Elektronegativiteit: Het zwavelatoom in zwavelzuur is elektronegatiever dan het stikstofatoom in salpeterzuur. Dit betekent dat zwavel elektronen sterker aantrekt, wat leidt tot een meer gepolariseerde O-H-binding en een grotere neiging om protonen vrij te geven.
* Resonantiestabilisatie: Het sulfaation (SO₄²⁻) is meer resonantiegestabiliseerd dan het nitraation (NO₃⁻). Deze stabilisatie maakt het gemakkelijker voor zwavelzuur om zijn protonen te verliezen.
Samengevat: Zwavelzuur heeft een grotere neiging om protonen te doneren, waardoor het een sterker zuur is dan salpeterzuur.
 Is een rots een levenloos object?
Is een rots een levenloos object?  Beste manier om klimaatverandering tegen te gaan? Plant een biljoen bomen
Beste manier om klimaatverandering tegen te gaan? Plant een biljoen bomen  Te koop:uniek stuk grond in strategische Arctische archipel
Te koop:uniek stuk grond in strategische Arctische archipel  Satellieten brengen koolstof in kaart die is vastgelegd door bossen, met een nauwkeurigheid tot tien meter
Satellieten brengen koolstof in kaart die is vastgelegd door bossen, met een nauwkeurigheid tot tien meter Betrouwbaar tropisch weerpatroon om te veranderen in een opwarmend klimaat
Betrouwbaar tropisch weerpatroon om te veranderen in een opwarmend klimaat
Hoofdlijnen
- Welke cellen bestrijden infectie?
- Wat is celinductie?
- De wetenschappelijke methode maakt gebruik van observatie en welk ander proces om de vragen te beantwoorden?
- Wat is een native eiwit?
- Welke term beschrijft alle veranderingen die plaatsvinden tijdens het leven van een organisme inclusief groei?
- Hoe zou u een microscoop kunnen gebruiken om te bepalen of het monster leven of niet-levend is?
- Welk systeem staat bekend als de wiskundige taal van anatomie en fysiologie?
- In welke vorm is het DNA aanwezig in een cel bij het niet delen?
- Welke organel van het endomembraansysteem geassocieerd met het sorteren van lipiden en eiwitten voor verschillende cellulaire functies zijn?
- Wereldprimeur voor het lezen van digitaal gecodeerde synthetische moleculen
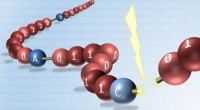
- Organische afstandhouders verbeteren de LED-prestaties
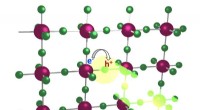
- Onderzoekers maken een magneet gemaakt van één molecuul
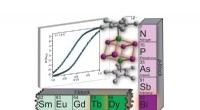
- Met gewone tape, onderzoekers maken chip die de ontwikkeling van medicijnen kan versnellen
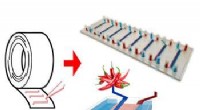
- Wetenschappers bieden bedrijven een nieuwe chemie voor groener polyurethaan

 De oorsprong van genen voor het maken van bloemen
De oorsprong van genen voor het maken van bloemen Waarom werden de sterren gemaakt?
Waarom werden de sterren gemaakt?  Toekomstige subtropische opwarming versnelt tropische klimaatverandering
Toekomstige subtropische opwarming versnelt tropische klimaatverandering Wat is de kleur van fluoriet?
Wat is de kleur van fluoriet?  Wat is het effect van te veel mijnbouw en steengroeves om doelbewust edele metalen, stenen, grind in natuurlijke hulpbronnen te verkrijgen?
Wat is het effect van te veel mijnbouw en steengroeves om doelbewust edele metalen, stenen, grind in natuurlijke hulpbronnen te verkrijgen?  Draadloos oplaadbare solid-state supercondensatoren printen voor zachte, slimme contactlenzen
Draadloos oplaadbare solid-state supercondensatoren printen voor zachte, slimme contactlenzen Ozon (O3):Covalente bindingen uitgelegd - Eigenschappen en structuur
Ozon (O3):Covalente bindingen uitgelegd - Eigenschappen en structuur  De edelgasconfiguratie voor nikkel-element?
De edelgasconfiguratie voor nikkel-element?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

