
Wetenschap
Ionische binding:elektronenoverdracht en ionenvorming uitgelegd
De basis
* Ionische bindingen komen voor tussen een metaal en een niet-metaal. Metalen hebben de neiging elektronen te verliezen, terwijl niet-metalen de neiging hebben elektronen te winnen.
* Elektronen worden overgedragen, niet gedeeld. Dit is een belangrijk verschil tussen ionische en covalente bindingen.
Het proces
1. Metaal verliest een elektron: Het metaalatoom, met zijn losjes vastgehouden elektronen, verliest een of meer elektronen. Hierdoor ontstaat een positief geladen ion (een kation genoemd).
2. Niet-metaal krijgt een elektron: Het niet-metaalatoom, met een sterk verlangen om zijn buitenste elektronenschil te voltooien, wint het (de) elektron(en) dat/die door het metaal verloren is/zijn. Hierdoor ontstaat een negatief geladen ion (een anion genoemd).
3. Elektrostatische aantrekkingskracht: De tegengesteld geladen ionen worden nu door elektrostatische krachten tot elkaar aangetrokken. Deze aantrekkingskracht houdt de ionen in de ionische verbinding bij elkaar.
Voorbeeld:natriumchloride (NaCl)
* Natrium (Na) , een metaal, verliest één elektron en wordt een natriumion (Na+).
* Chloor (Cl) , een niet-metaal, verkrijgt het elektron om een chloride-ion (Cl-) te worden.
* De tegengesteld geladen ionen (Na+ en Cl-) trekken elkaar aan, vormen een ionische binding en creëren de verbinding natriumchloride (NaCl).
Belangrijkste punten
* De overdracht van elektronen is wat ionische binding definieert.
* De resulterende ionen hebben volledige buitenste elektronenschillen, waardoor ze stabieler zijn.
* De sterke elektrostatische aantrekkingskracht tussen de ionen leidt tot een verbinding met een hoog smeltpunt en hoog kookpunt.
Laat het me weten als je meer informatie wilt of andere vragen hebt!
 Klimaatchaos vermijden betekent ongekende verandering:VN-rapport
Klimaatchaos vermijden betekent ongekende verandering:VN-rapport Kijk eerst naar een duurzame landbouwmulch
Kijk eerst naar een duurzame landbouwmulch Nieuw onderzoek laat zien hoe onderzees grondwater de groei van koraalriffen beïnvloedt
Nieuw onderzoek laat zien hoe onderzees grondwater de groei van koraalriffen beïnvloedt Zijn otters carnivore, omnivore of herbivoor?
Zijn otters carnivore, omnivore of herbivoor?  Uit onderzoek blijkt dat een deel van India een klimaathotspot zal worden
Uit onderzoek blijkt dat een deel van India een klimaathotspot zal worden
Hoofdlijnen
- Ziek van de Mexicaanse griep? Giftige algen kunnen de volgende grote bedreiging zijn
- Waar hoort Psilophyta bij de fylogenie?
- Wat voor soort planten eten maïsoorwormen?
- Wat zijn de vergelijkbare kenmerken die hun oorsprong vinden in een gedeelde voorouder?
- Wat voor soort selectie kan leiden tot speciatie?
- Wat zijn specifieke celtypen?
- Hoe wordt de manier waarop Hox -genen tot expressie worden gebracht bij muizen die verschillen van hun fruitvliegen?
- Archaea: Structure, Characteristics & Domain
- Wat een specimencollectie helpt een wetenschapper onderzoek te doen?
- Goedkoop chip-gebaseerd apparaat kan spectrometrie transformeren

- Toppen van waterige golven kunnen essentiële chemicaliën transporteren in een industrieel scheidingsproces
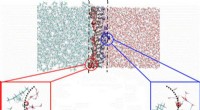
- Apparaat kan tekenen van buitenaards leven helpen detecteren

- Elektrische schok tot koolstof maakt een betere waterzuiveraar
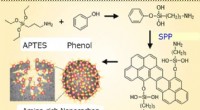
- Onderzoek vooruitgang zoeken naar nieuwe antibiotica
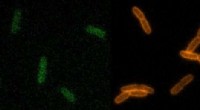
 Een wortel is een voorbeeld van wat voor soort wortel?
Een wortel is een voorbeeld van wat voor soort wortel?  Levensveranderend of oplichting? Axie Infinity helpt arme Filipijnen te verdienen
Levensveranderend of oplichting? Axie Infinity helpt arme Filipijnen te verdienen Een stof met een pH van 11 is welke tijden meer dan 8?
Een stof met een pH van 11 is welke tijden meer dan 8?  Methanol in waterige oplossingen:oplosbaarheid begrijpen
Methanol in waterige oplossingen:oplosbaarheid begrijpen  Kunnen insecten dik worden?
Kunnen insecten dik worden? UITLEG:Terwijl de rook van bosbranden zich verspreidt, wie loopt er gevaar?
UITLEG:Terwijl de rook van bosbranden zich verspreidt, wie loopt er gevaar? Hoe beïnvloedt de lensdikte de brandpuntsafstand?
Hoe beïnvloedt de lensdikte de brandpuntsafstand?  Immigranten die misdrijven hebben gepleegd, hebben minder kans dan niet-immigranten om nog een misdrijf te plegen
Immigranten die misdrijven hebben gepleegd, hebben minder kans dan niet-immigranten om nog een misdrijf te plegen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

