
Wetenschap
Kationen in ionische binding:metaalgedrag begrijpen
* Metalen hebben een lage elektronegativiteit: Ze hebben een zwakkere greep op hun valentie-elektronen.
* Niet-metalen hebben een hoge elektronegativiteit: Ze hebben een sterke aantrekkingskracht op elektronen.
Wanneer een metaal en een niet-metaal ionisch binden, *verliest* het metaalatoom één of meer elektronen om een positief geladen ion (kation) te worden. Het niet-metaalatoom *verkrijgt* die elektronen en wordt een negatief geladen ion (anion).
Voorbeeld: In natriumchloride (NaCl) is natrium (Na) een metaal en chloor (Cl) een niet-metaal. Natrium verliest een elektron om een natriumkation (Na+) te worden, terwijl chloor dat elektron wint om een chloride-anion (Cl-) te worden. De tegengestelde ladingen trekken elkaar aan en vormen de ionische verbinding.
 Hoe het gewicht van water te berekenen
Hoe het gewicht van water te berekenen Commerciële waterstof wordt verkregen uit welk gas?
Commerciële waterstof wordt verkregen uit welk gas?  Nieuwe röntgenspectroscopie onderzoekt waterstofgenererende katalysator
Nieuwe röntgenspectroscopie onderzoekt waterstofgenererende katalysator Welke verbinding heeft het hoogste percentage koolstof per massa?
Welke verbinding heeft het hoogste percentage koolstof per massa?  Wetenschappers ontwikkelen efficiënter katalytisch materiaal voor brandstofceltoepassingen
Wetenschappers ontwikkelen efficiënter katalytisch materiaal voor brandstofceltoepassingen
 NASA identificeert een sterke tropische cycloon in de Arabische Zee Kyarr
NASA identificeert een sterke tropische cycloon in de Arabische Zee Kyarr Geowetenschappers documenteren de rol van atmosferisch stof op mariene ecosystemen 300 miljoen jaar geleden
Geowetenschappers documenteren de rol van atmosferisch stof op mariene ecosystemen 300 miljoen jaar geleden Wanneer was van kleine dingen grote groei gecreëerd?
Wanneer was van kleine dingen grote groei gecreëerd?  Apparaten om verontreinigende stoffen uit rookstapels te verwijderen
Apparaten om verontreinigende stoffen uit rookstapels te verwijderen  Wat is een dubbele aard?
Wat is een dubbele aard?
Hoofdlijnen
- Ribosomen: definitie, functie en structuur (eukaryoten en prokaryoten)
- Hoe zou je een grote koloniale organismen onderscheiden van meercellig organisme?
- Het deel van de plant dat suikers transporteert geproduceerd door fotosynthese naar niet-groene delen is de?
- Is een rode kangoeroe -multicellulair organisme?
- Het orgaan in het lichaam absorbeert meer water is groot Instestine?
- Welke nucleotiden koppelen samen?
- Hoe wordt het genoemd toen DNA werd opgeknapt in het verdelen van cellen?
- Waarom verspreiden bloeiende planten hun zaden?
- Hoeveel enzymen zijn er geïdentificeerd?
- Supraballs bieden een nieuwe manier om materialen te kleuren

- Onderzoek naar met stikstof gedoteerde polycyclische aromatische koolwaterstoffen voor hoogwaardige OLED's

- Materiaalwetenschappers laten zien hoe duurzame kunstpezen kunnen worden gemaakt van verbeterde hydrogels

- Onderzoek naar nieuwe medicijnen kan de behoefte aan proefdieren drastisch verminderen
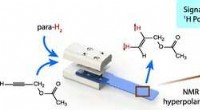
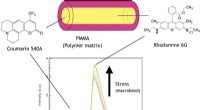
- Op polymeer gebaseerde optische vezel voor visualisatie van materiaalspanning
 Is het een chemische reactie als je maar koper in vuur en zwart wordt?
Is het een chemische reactie als je maar koper in vuur en zwart wordt?  Acute tastzin helpt kolibries dichtbij een bloem te zweven zonder er tegenaan te botsen, blijkt uit onderzoek
Acute tastzin helpt kolibries dichtbij een bloem te zweven zonder er tegenaan te botsen, blijkt uit onderzoek  Amerikaanse wetgevers starten debat over online privacy
Amerikaanse wetgevers starten debat over online privacy Een aanpak om de uitleg van machine learning te verbeteren
Een aanpak om de uitleg van machine learning te verbeteren Tropische cycloon Joyce die de kust van Noordwest-Australië doorweekt
Tropische cycloon Joyce die de kust van Noordwest-Australië doorweekt New Jersey keurt gasleiding door beschermd Pinelands goed
New Jersey keurt gasleiding door beschermd Pinelands goed Is astrologisch symbool en astronomie hetzelfde?
Is astrologisch symbool en astronomie hetzelfde?  Wetenschappers draaien evolutionaire klok terug om CO2-tolerante microalgen te ontwikkelen
Wetenschappers draaien evolutionaire klok terug om CO2-tolerante microalgen te ontwikkelen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

