
Wetenschap
Hybridisatie van Cl₂O:een stapsgewijze handleiding
1. Teken de Lewis-structuur
* Valentie-elektronen tellen: Chloor (Cl) heeft 7 valentie-elektronen en zuurstof (O) heeft er 6. Met twee chlooratomen is het totaal 7 + 7 + 6 =20 valentie-elektronen.
* Verbind de atomen: Plaats het zuurstofatoom in het midden, omdat het minder elektronegatief is. Verbind het met de twee chlooratomen met enkele bindingen.
* Volledige octetten: Elk chlooratoom heeft nog 6 elektronen nodig, en het zuurstofatoom heeft er nog 4 nodig. Hiervoor zijn twee alleenstaande paren op elk chlooratoom en twee alleenstaande paren op het zuurstofatoom nodig.
2. Bepaal het sterische getal
* Sterisch getal: Dit is het aantal elektronengroepen rond het centrale atoom. Elektronengroepen omvatten bindingen (enkel, dubbel of drievoudig) en alleenstaande paren.
* In Cl₂O: Het zuurstofatoom heeft twee bindingen (met de chlooratomen) en twee alleenstaande paren, waardoor het een sterisch getal van 4 krijgt.
3. Breng het sterische getal in verband met hybridisatie
* Sterisch getal | Hybridisatie
* 2 | sp
* 3 | sp²
* 4 | sp³
* 5 | sp³d
* 6 | sp³d²
4. Conclusie
Omdat het centrale zuurstofatoom in Cl₂O een sterisch getal van 4 heeft, is de hybridisatie sp³ .
 Vernietigt de opwarming van de aarde de Mount Everest?
Vernietigt de opwarming van de aarde de Mount Everest?  Het heilige meer opruimen:locals pakken vervuiling door Titicaca aan
Het heilige meer opruimen:locals pakken vervuiling door Titicaca aan Wat is de prooi in een ecosysteem?
Wat is de prooi in een ecosysteem?  Instabiliteit in Antarctisch ijs zal naar verwachting de zeespiegel snel doen stijgen
Instabiliteit in Antarctisch ijs zal naar verwachting de zeespiegel snel doen stijgen Actie ondernemen om Net Zero in de landbouwsector te bereiken
Actie ondernemen om Net Zero in de landbouwsector te bereiken
Hoofdlijnen
- Wat bepaalt de specifieke kenmerken van een organisme op een chromosoom?
- Wat is het maag -enzym dat op eiwitten werkt?
- Onderzoek onderzoekt hoe druivenplagen bessen opsnuiven
- Vul de blanco A in een celgedeelte dat alleen planten kern of celwand hebben die het?
- Welke reproductieve cyclus vernietigt de gastheercel niet?
- Mutaties? - Antwoorden
- Zodra een organisme een wetenschappelijke naam heeft, kan het niet worden gewijzigd?
- EP-leden dringen aan op onderzoek naar de invloed van Monsanto op onderzoek
- Is symbiose een nauwe relatie tussen twee gemeenschappen?
- Onderzoekers ontwikkelen thermo-responsieve eiwithydrogel
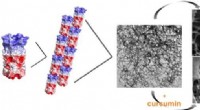
- Onderzoeksteam reconstrueert motorvrachtcomplex voor ciliair transport

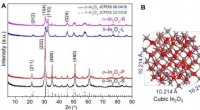
- Efficiënte indiumoxidekatalysatoren ontworpen voor CO2-hydrogenering tot methanol
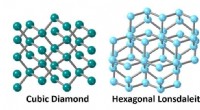
- We hebben in minuten zonder hitte diamanten gemaakt door de kracht van een asteroïdebotsing na te bootsen
- Beheersing van chemische reacties nabij het absolute nulpunt

 Zijn verbindingen willekeurige combinaties van elementen?
Zijn verbindingen willekeurige combinaties van elementen?  Zwakke zure ionisatie:gedeeltelijke dissociatie begrijpen
Zwakke zure ionisatie:gedeeltelijke dissociatie begrijpen  3 Hoofdbiomen alleen in het Amerikaanse land?
3 Hoofdbiomen alleen in het Amerikaanse land?  Air France moet profiteren van thuismarkt:AF-KLM-chef
Air France moet profiteren van thuismarkt:AF-KLM-chef Wat zijn de drie dingen die in de bodem worden gevonden?
Wat zijn de drie dingen die in de bodem worden gevonden?  Welk organisme wordt het minst beïnvloed door afwezigheid van zonlicht?
Welk organisme wordt het minst beïnvloed door afwezigheid van zonlicht?  Ribosomen nemen deel aan het proces van?
Ribosomen nemen deel aan het proces van?  Wordt energie gewonnen of verloren wanneer het van kinetische naar thermische wrijving omzet?
Wordt energie gewonnen of verloren wanneer het van kinetische naar thermische wrijving omzet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

