
Wetenschap
Zwakke zure ionisatie:gedeeltelijke dissociatie begrijpen
Hier is een overzicht van wat er gebeurt:
1. Het zwakke zuurmolecuul (HA) is in evenwicht met zijn geconjugeerde base (A-) en een waterstofion (H+):
```
HA(aq) ⇌ H+(aq) + A-(aq)
```
2. Het evenwicht ligt ver naar links: Dit betekent dat het grootste deel van het zwakke zuur ongedissocieerd blijft. Er is slechts een kleine hoeveelheid H+- en A-ionen in de oplossing aanwezig.
3. De mate van ionisatie wordt weergegeven door de zuurdissociatieconstante (Ka):
```
Ka =[H+][A-] / [HA]
```
Een kleinere Ka-waarde duidt op een zwakker zuur, wat betekent dat het minder ioniseert.
Gevolgen van zwakke zuurionisatie:
* Lagere concentratie waterstofionen: Zwakke zuren produceren een lagere concentratie H+-ionen in oplossing vergeleken met sterke zuren. Dit resulteert in een hogere pH waarde.
* Buffercapaciteit: Zwakke zuren kunnen, samen met hun geconjugeerde basen, fungeren als buffers en weerstand bieden aan veranderingen in de pH wanneer kleine hoeveelheden zuur of base aan de oplossing worden toegevoegd.
* Verschillende chemische reacties: De gedeeltelijke ionisatie van zwakke zuren kan het verloop van chemische reacties beïnvloeden, omdat de concentratie van H+-ionen lager is in vergelijking met sterke zuren.
Voorbeeld:
Azijnzuur (CH3COOH) is een zwak zuur. In water valt het gedeeltelijk uiteen in acetaationen (CH3COO-) en waterstofionen (H+):
```
CH3COOH(aq) ⇌ H+(aq) + CH3COO-(aq)
```
Slechts een klein deel van de azijnzuurmoleculen ioniseert daadwerkelijk, wat resulteert in een lagere concentratie H+-ionen en een hogere pH vergeleken met een sterk zuur zoals zoutzuur (HCl).
Samengevat: De ionisatie van een zwak zuur is een omkeerbaar proces met een evenwicht dat de niet-gedissocieerde zuurvorm bevoordeelt. Dit resulteert in een lagere concentratie H+-ionen, een hogere pH en de mogelijkheid tot bufferende werking.
 Bestaande klimaatmodellen nuttig bij het voorspellen, model testen
Bestaande klimaatmodellen nuttig bij het voorspellen, model testen Wat is een bepaalde rol in een ecosysteem of hoe het zijn leven verdient?
Wat is een bepaalde rol in een ecosysteem of hoe het zijn leven verdient?  Experiment suggereert dat silicium ontbreekt in de kern van de aarde
Experiment suggereert dat silicium ontbreekt in de kern van de aarde Wat zijn natuurlijke gebeurtenissen?
Wat zijn natuurlijke gebeurtenissen?  Nieuw onderzoek suggereert dat de wereldwijde ijstijd het gezicht van de planeet heeft veranderd
Nieuw onderzoek suggereert dat de wereldwijde ijstijd het gezicht van de planeet heeft veranderd
Hoofdlijnen
- Wat gebeurt er als we menselijke kwaliteiten toekennen aan bedrijven?
- Virtuele Labrador kan onderzoekers helpen bij het aanpakken van hondenbeten
- Wat is het product van DNA -transcriptie?
- Welk voedsel bevat geen lipiden?
- De tool die leidt tot de begrip van cellen zijn basiseenheid van het leven was de?
- Wat zijn de rollen van chromosomen -DNA en genen bij het opslaan van genetisch materiaal?
- Welke cellen hebben isotone oplossingen nodig om bij homeostase te zijn?
- Wat is een reactant in biologische termen?
- Project om het publiek toegang te geven tot 3D-modellen met hoge resolutie van de anatomie van gewervelde dieren
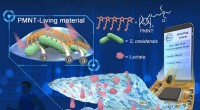
- Flexibel bio-elektronisch apparaat op basis van levend materiaal voor het monitoren van lactaat- en tumorcellen
- Onderzoekers werken samen met kleine bedrijven in NM om nieuwe beademingsmaterialen te testen

- Hybride fotoactieve perovskieten voor het eerst gefotografeerd met atomaire resolutie

- Microfluïdische array-vangsten, houdt enkele cervicale cellen vast voor snellere screening

- Less is more:een zachte, zelfaangedreven pomp om mechatronische apparaten te vereenvoudigen
 Wat is het lichtbereik van vergroting?
Wat is het lichtbereik van vergroting?  Wat was de bijdrage van Alexander Fleming in Science Biology?
Wat was de bijdrage van Alexander Fleming in Science Biology?  Wat zijn de basisprincipes van Mendeliaanse genetica?
Wat zijn de basisprincipes van Mendeliaanse genetica?  Wordt chloor door planten gebruikt voor fotosynthese?
Wordt chloor door planten gebruikt voor fotosynthese?  Hoe dosis 100 m² lijken eruit?
Hoe dosis 100 m² lijken eruit?  Seismische sensoren registreren orkaanintensiteit, studie vondsten
Seismische sensoren registreren orkaanintensiteit, studie vondsten Afbeelding:Kleine satelliet demonstreert mogelijke oplossing voor ruimteafval
Afbeelding:Kleine satelliet demonstreert mogelijke oplossing voor ruimteafval Een habitat maken voor een schoolproject
Een habitat maken voor een schoolproject
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

