
Wetenschap
Edelgassen:waarom ze geen chemische bindingen vormen
Dit is waarom:
* Volledige schelpen: Edelgassen hebben een volledige buitenste elektronenschil (ook bekend als de valentieschil). Dit betekent dat ze een stabiele elektronenconfiguratie hebben en geen elektronen hoeven te winnen of te verliezen om een volledige schil te bereiken.
* Lage reactiviteit: Hun stabiele elektronenconfiguratie maakt ze zeer onreactief. Ze vormen niet gemakkelijk verbindingen met andere elementen.
Voorbeelden van edelgassen zijn onder meer:
* Helium (hij)
* Neon (Ne)
* Argon (Ar)
* Krypton (Kr)
* Xenon (Xe)
* Radon (Rn)
Hoewel ooit werd gedacht dat edelgassen volledig inert waren, hebben wetenschappers ontdekt dat sommige edelgassen onder specifieke omstandigheden verbindingen kunnen vormen, vooral met zeer elektronegatieve elementen zoals fluor. Deze verbindingen zijn echter over het algemeen zeer onstabiel.
 Probes werpen nieuw licht op de oorzaak van Alzheimer
Probes werpen nieuw licht op de oorzaak van Alzheimer Grote kristallen uit wateroplossingen vormen meestal een zeer snelle koeling waar of onwaar?
Grote kristallen uit wateroplossingen vormen meestal een zeer snelle koeling waar of onwaar?  Welke mineraal vormt wanneer chloorjodiumbroom en fluorcombinatie?
Welke mineraal vormt wanneer chloorjodiumbroom en fluorcombinatie?  Belangrijkste mechanismen van luchtwegontspanning bij astma onthuld in nieuwe studie
Belangrijkste mechanismen van luchtwegontspanning bij astma onthuld in nieuwe studie Ingenieurs 3D printen zeer sterk aluminium, los eeuwenoud lasprobleem op met nanodeeltjes
Ingenieurs 3D printen zeer sterk aluminium, los eeuwenoud lasprobleem op met nanodeeltjes
 Opruimen van vervuiling door mijnbouw in een rivier die op de Werelderfgoedlijst staat
Opruimen van vervuiling door mijnbouw in een rivier die op de Werelderfgoedlijst staat Studie test de veerkracht van de Salish Sea tegen de gevolgen van klimaatverandering
Studie test de veerkracht van de Salish Sea tegen de gevolgen van klimaatverandering NASA vangt tropische depressie Pilar die de kust van Mexico omhelst en onderdompelt
NASA vangt tropische depressie Pilar die de kust van Mexico omhelst en onderdompelt Door voedselproductie gedreven landgebruik leidt tot veranderingen in watergerelateerde ecosysteemdiensten
Door voedselproductie gedreven landgebruik leidt tot veranderingen in watergerelateerde ecosysteemdiensten Oogsten in de VS lijden onder klimaatverandering, volgens studie
Oogsten in de VS lijden onder klimaatverandering, volgens studie
Hoofdlijnen
- Ingewikkelde ijsgrotten in Antarctica May Harbor Unique Life
- Onderzoek toont gedragsveranderingen, fysiologische veranderingen bij mieren die verstoord zijn door ontwikkeling, stadsuitbreiding
- In welk bioom zit de cyclops eronder?
- Wat zijn de delen van cel die in dierlijke cellen worden gevonden die geen plantencellen planten?
- De gezondheidsvoordelen van medische marihuana:een uitgebreid overzicht
- Wat hebben cellen en weefsels gemeen?
- Wat is lathyogeen?
- Draagt lichaamsbeweging ontwikkeling aan? Bij de zeeanemoon is de manier waarop je beweegt van belang
- Hoe helpt de analogie van een cel naar de stad u te begrijpen waarom cellen zich verdelen?
- Inheemse Nieuw-Zeelandse boom doet pijn

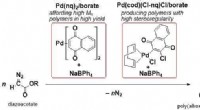
- Nieuwe op palladium gebaseerde initiatiesystemen voor C1-polymerisatie van diazoacetaten
- Onderzoekers tonen aan dat organische kristallen kunnen dienen als energieomzetters voor opkomende technologieën

- Video:Waarom limoensap je huid verbrandt in de zon

- Doorbraak in synthese van scheikundigen bevordert een krachtig middel tegen kanker

 Wat gebruiken stikstoffixerende bacteriën om gasmoleculen te splitsen en de atomen te combineren met waterstof?
Wat gebruiken stikstoffixerende bacteriën om gasmoleculen te splitsen en de atomen te combineren met waterstof?  Geleerde lessen bij het maken van biomedische nanodeeltjes voor menselijk gebruik
Geleerde lessen bij het maken van biomedische nanodeeltjes voor menselijk gebruik Symboolvergelijking Wanneer koperen carbonaat wordt verwarmd?
Symboolvergelijking Wanneer koperen carbonaat wordt verwarmd?  Waarom beschouw je de gasvormige toestand van water als dampen terwijl dat ammoniakgas?
Waarom beschouw je de gasvormige toestand van water als dampen terwijl dat ammoniakgas?  Aanbevelingen voor het creëren van een afdeling Duurzaamheid en Klimaatverandering in NYC
Aanbevelingen voor het creëren van een afdeling Duurzaamheid en Klimaatverandering in NYC Geen duidelijk vluchtplan voor Alitalia na stilstand van reddingsacties
Geen duidelijk vluchtplan voor Alitalia na stilstand van reddingsacties Tropische regenwouden voor kinderen
Tropische regenwouden voor kinderen Waarom magnetisme in bepaalde materialen anders is in atomair dunne lagen en hun bulkvormen?
Waarom magnetisme in bepaalde materialen anders is in atomair dunne lagen en hun bulkvormen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

