
Wetenschap
Verspreidingssnelheden:vergelijking van ammoniak (NH₃) en waterstofchloride (HCl)
Zowel ammoniak- (NH₃) als waterstofchloride-gassen (HCl) diffunderen, maar waterstofchloride (HCl) diffundeert sneller .
Dit is waarom:
* Grahams wet van diffusie: Deze wet stelt dat de diffusiesnelheid van een gas omgekeerd evenredig is met de vierkantswortel van zijn molaire massa.
* Molaarmassa: De molaire massa van HCl (36,46 g/mol) is lager dan de molaire massa van ammoniak (17,03 g/mol).
* Verspreidingssnelheid: Omdat HCl een lagere molmassa heeft, zal het sneller diffunderen dan ammoniak.
In eenvoudiger bewoordingen: Lichtere moleculen bewegen sneller en verspreiden zich sneller dan zwaardere moleculen.
Hoofdlijnen
- Invasieve uitheemse soorten? Is daar geen app voor?
- Welke organismen reproduceren snel resulterend uiteindelijk in een gebrek aan zuurstof?
- Wie ontwikkelde de Theroy of Evolution?
- Hoe hashtags en @-symbolen de taal op Twitter beïnvloeden
- Welke veranderingen in de cellulaire ademhaling kun je verwachten in slapende zaden?
- Instructies van DNA worden in eiwitten vertaald door organellen die wat worden genoemd?
- Welk type cellen omringen vasculair weefsel een plantenstam?
- Het vermogen van een organisme om zijn tolerantieniveau abiotische factoren aan te passen?
- Linnaean-classificatie: definitie, niveaus en voorbeelden (met grafiek)
- Chemici ontdekken hoe blauw licht blindheid versnelt

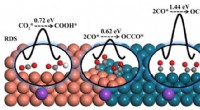
- Afstemming van reactiebarrières voor elektroreductie van kooldioxide tot producten met meerdere koolstofatomen
- Onderzoekers ontdekken nieuwe transportroute voor vluchtige plantenstoffen

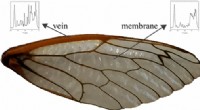
- Hoe krekels erin slagen om het te vleugelen
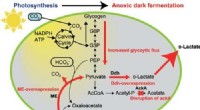
- Methode levert een hoog percentage D-lactaat op met behulp van cyanobacteriën, kan een revolutie teweegbrengen in de productie van bioplastic
 Big data spelen een grote rol bij de Amerikaanse presidentsverkiezingen. Hebben ze dezelfde impact in Australië?
Big data spelen een grote rol bij de Amerikaanse presidentsverkiezingen. Hebben ze dezelfde impact in Australië?  Welke term betekent onder invloed van de zon?
Welke term betekent onder invloed van de zon?  Heeft de Blue Main-Sequence-ster een langer leven dan andere sterren?
Heeft de Blue Main-Sequence-ster een langer leven dan andere sterren?  Oude voedselwebben kunnen duurzame toekomsten in kaart brengen
Oude voedselwebben kunnen duurzame toekomsten in kaart brengen Sucrose-polariteit:de eigenschappen en structuur ervan begrijpen
Sucrose-polariteit:de eigenschappen en structuur ervan begrijpen  Wat is een andere naam voor een gewone microscoop?
Wat is een andere naam voor een gewone microscoop?  Welke celstructuur was niet te zien totdat de elektronenmicroscoop was uitgevonden?
Welke celstructuur was niet te zien totdat de elektronenmicroscoop was uitgevonden?  Onderzoeker onderzoekt het potentieel van grafeen
Onderzoeker onderzoekt het potentieel van grafeen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


