
Wetenschap
Oplosbaarheid van ijzerhydroxide:inzicht in de optimale pH
* Fe(OH)₃ is een zwakke base: Het reageert met zuren en vormt oplosbare zouten.
* Het principe van Le Chatelier: Wanneer een zuur wordt toegevoegd, reageert dit met de hydroxide-ionen (OH-) uit Fe(OH)3. Deze reactie verschuift het evenwicht en bevordert het oplossen van meer Fe(OH)3 ter vervanging van de verbruikte OH-ionen.
Voorbeeld:
Fe(OH)₃(s) + 3H⁺(aq) ⇌ Fe³⁺(aq) + 3H₂O(l)
Door een sterk zuur zoals HCl toe te voegen, zullen de H⁺-ionen reageren met de OH⁻-ionen, waardoor het evenwicht naar rechts wordt verschoven en de oplosbaarheid van Fe(OH)₃ toeneemt.
Belangrijke opmerking: Hoewel zure oplossingen de oplosbaarheid verhogen, kan een extreem hoge zuurgraad leiden tot de vorming van andere complexen, die de oplosbaarheid van Fe(OH)₃ zouden kunnen verminderen.
 Chemici ontwikkelen nieuw materiaal waarmee slim glas in recordtijd van kleur kan veranderen
Chemici ontwikkelen nieuw materiaal waarmee slim glas in recordtijd van kleur kan veranderen Wat zijn de kleuren van chloor?
Wat zijn de kleuren van chloor?  Waarom lost de Alka Seltzer sneller op in frisdrank dan water?
Waarom lost de Alka Seltzer sneller op in frisdrank dan water?  Wordt waterstofgas net gecombineerd met zuurstof?
Wordt waterstofgas net gecombineerd met zuurstof?  Hoeveel componenten zijn er in zout en water wanneer gecombineerd?
Hoeveel componenten zijn er in zout en water wanneer gecombineerd?
 De snelle reactie van de staat Washington om invasieve moordhorzels uit te roeien
De snelle reactie van de staat Washington om invasieve moordhorzels uit te roeien  Vulkaan Hawaï kan rotsblokken ter grootte van koelkasten uitspuwen
Vulkaan Hawaï kan rotsblokken ter grootte van koelkasten uitspuwen Waarom deze plantenetende dinosaurus bloeide en zijn tijdperk domineerde
Waarom deze plantenetende dinosaurus bloeide en zijn tijdperk domineerde  Afbeelding:Japanse archipel en de westelijke Stille Oceaan
Afbeelding:Japanse archipel en de westelijke Stille Oceaan Waar is steenkool gevonden?
Waar is steenkool gevonden?
Hoofdlijnen
- Wat gebruikt een cel fermentatie in plaats van cellulaire ademhaling?
- Hoe noemen biologen de populaties van vele soorten die een bepaalde plaats innemen?
- Welke eigenschappen delen het jodendom en de islam?
- The Differences Between Clams & Scallops
- Het vreemde geval van de duikvlieg
- Zijn cellen meestal gemaakt van water?
- Wat wordt gezamenlijk de lichaamsbuis in een microscoop genoemd?
- De basiseenheid van organisatie nerveus weefsel is de zenuwcel of?
- G2-fase van de celcyclus:essentiële controles vóór mitose
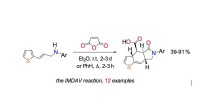
- Chemici suggereren een nieuwe manier om steroïde-analogen te synthetiseren
- Mollen beheersen in de chemie:een praktische gids voor molaire massa en stoichiometrie

- De geheimen van secundaire metabolieten extraheren
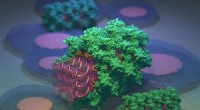
- DNA-nanostructuren worden gecamoufleerd door eiwitten
- Radicaal nieuw behandelingssysteem verlicht kankertherapie
 Het vulkanische eiland Japan kan de sleutel zijn tot het overleven van koraal
Het vulkanische eiland Japan kan de sleutel zijn tot het overleven van koraal Hoe vind je het aantal ongepaarde elektronen?
Hoe vind je het aantal ongepaarde elektronen?  Waar zijn de beste plaatsen om zonne -energie te gebruiken?
Waar zijn de beste plaatsen om zonne -energie te gebruiken?  Wat zijn de aanpassingen van de bladbug?
Wat zijn de aanpassingen van de bladbug?  Voordelen en nadelen van het recyclen van Metal
Voordelen en nadelen van het recyclen van Metal Wat gebeurt er met plasmalogenen, de fosfolipiden waar niemand graag aan denkt
Wat gebeurt er met plasmalogenen, de fosfolipiden waar niemand graag aan denkt  FTC klaagt aan om Harry's verkoop aan Schick-eigenaar Edgewell te blokkeren
FTC klaagt aan om Harry's verkoop aan Schick-eigenaar Edgewell te blokkeren Hoe te spanningsregulatie berekenen
Hoe te spanningsregulatie berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

