
Wetenschap
Sulfaation (SO₄²⁻):vorm, verbindingshoek en structuur uitgelegd
Dit is waarom:
* Centraal atoom: Het centrale atoom is zwavel (S).
* Omringende atomen: Vier zuurstofatomen (O) zijn gebonden aan het zwavelatoom.
* Elektronenparen: Zwavel heeft zes valentie-elektronen en elk zuurstofatoom draagt één elektron bij om een covalente binding te vormen. Dit geeft een totaal van 12 valentie-elektronen. Deze elektronen zijn gerangschikt in vier bindingsparen en twee alleenstaande paren rond het zwavelatoom.
* VSEPR-theorie: De vier bindingsparen en twee alleenstaande paren rond zwavel resulteren in een tetraëdrische elektronengeometrie. De afstoting tussen de elektronenparen duwt de bindingsparen dichter bij elkaar, wat leidt tot een iets kleinere bindingshoek dan de ideale 109,5°.
Visuele weergave:
Je kunt dit visualiseren door je een piramide voor te stellen met vier vlakken en een zwavelatoom in het midden. De vier zuurstofatomen bezetten de vier hoeken van de piramide.
 Hoe we van een golfbaan een toevluchtsoord maakten voor zeldzame salamanders, kikkers en padden
Hoe we van een golfbaan een toevluchtsoord maakten voor zeldzame salamanders, kikkers en padden  Vijfde van het voedsel ter wereld dat verloren gaat door te veel eten en verspillen, studie vondsten
Vijfde van het voedsel ter wereld dat verloren gaat door te veel eten en verspillen, studie vondsten Onderzoekers bestuderen Golf van Mexico in internationale samenwerking
Onderzoekers bestuderen Golf van Mexico in internationale samenwerking Voorspellen en beheersen van dioxines
Voorspellen en beheersen van dioxines Onderzoekers krijgen nieuwe inzichten over rivierdynamiek
Onderzoekers krijgen nieuwe inzichten over rivierdynamiek
Hoofdlijnen
- Wat is apoptose?
- Wie heeft de kern uitgevonden?
- Wat zijn 3 mechanismen en aanpassingen voor zaadverspreiding?
- Wat betekent niet -reproductieve cellen?
- Wat is de belangrijkste taak die micro -organismen doen?
- Nieuwe Dehalogenimonas sp. stam kan dechlorering van diclofenac stimuleren
- Welke weefseltypen blijven tijdens het leven zeer mitotisch en waarom?
- Wat transporteert zuurstof naar cellen in het lichaam?
- Waarom binden enzymen over het algemeen slechts aan één type substraat?
- COF-999:een poreus poeder dat CO₂ rechtstreeks uit de omgevingslucht opvangt

- Nieuwe studie presenteert zeer actieve ozygenated groepen in koolstofmaterialen voor zuurstofreductie tot waterstofperoxide

- Chemici gebruiken licht om biologisch actieve verbindingen te bouwen

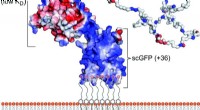
- Kunstmatige membraanbindende eiwitten om stamcellen naar het myocardium te leiden
- Synchrotron onthult belangrijke informatie over het beroemde beeldhouwwerk van Paul Gauguin

 Hoe wordt recombinant DNA gemaakt?
Hoe wordt recombinant DNA gemaakt?  Wat is Dukono -plaattektoniek?
Wat is Dukono -plaattektoniek?  Stijgende oceaantemperaturen bedreigen zeegrasweiden en hun vermogen om koolstof vast te houden
Stijgende oceaantemperaturen bedreigen zeegrasweiden en hun vermogen om koolstof vast te houden Wat is de zwaartekracht in een bewegend object?
Wat is de zwaartekracht in een bewegend object?  AI-aangedreven microscoop kan binnen enkele minuten kankermarges controleren
AI-aangedreven microscoop kan binnen enkele minuten kankermarges controleren Waarom zijn diepe waterstromingen belangrijk?
Waarom zijn diepe waterstromingen belangrijk?  Welke bereiken op de pH -schaal zijn zure basis en neutraal?
Welke bereiken op de pH -schaal zijn zure basis en neutraal?  Inzicht in de verrijking van uranium:processen, toepassingen en de toenemende zorgen van Iran
Inzicht in de verrijking van uranium:processen, toepassingen en de toenemende zorgen van Iran
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

