
Wetenschap
Kooldioxide- en kalkwaterreactie:een gedetailleerde uitleg
Hier ziet u hoe de reactie plaatsvindt:
1. Kalkwater is een heldere, kleurloze oplossing van calciumhydroxide ($Ca(OH)_2$) in water.
2. Kooldioxide is een kleurloos, geurloos gas.
3. Wanneer koolstofdioxide door kalkwater wordt geborreld, lost het op in het water en reageert het met het calciumhydroxide om calciumcarbonaat en water te vormen:
$CO_2(g) + Ca(OH)_2(aq) \rightarrow CaCO_3(s) + H_2O(l)$
4. Calciumcarbonaat is een witte, onoplosbare vaste stof, die in de oplossing als een melkachtig wit neerslag verschijnt. Hierdoor wordt het kalkwater troebel.
De reactie is omkeerbaar:
Als je kooldioxide door het kalkwater blijft borrelen, zal het melkwitte neerslag uiteindelijk oplossen. Dit komt omdat de overtollige koolstofdioxide zal reageren met het calciumcarbonaat en calciumbicarbonaat ($Ca(HCO_3)_2$) zal vormen, dat oplosbaar is in water:
$CaCO_3(s) + CO_2(g) + H_2O(l) \rechterpijl Ca(HCO_3)_2(aq)$
Samengevat:
* Kooldioxide dat reageert met kalkwater resulteert in de vorming van een melkachtig wit neerslag van calciumcarbonaat, wat een kenmerkende indicatie is voor de aanwezigheid van kooldioxide.
* De reactie is omkeerbaar en overtollig kooldioxide kan het neerslag oplossen.
 Hoe wordt groene nanotechnologie gebruikt?
Hoe wordt groene nanotechnologie gebruikt?  Middellandse-Zeegebied zwaar getroffen door klimaatverandering:studie
Middellandse-Zeegebied zwaar getroffen door klimaatverandering:studie Welk effect heeft een afname van zonlicht op het vijver -ecosysteem?
Welk effect heeft een afname van zonlicht op het vijver -ecosysteem?  Vier decennia aan gegevens klinkt vroegtijdige waarschuwing op Lake George
Vier decennia aan gegevens klinkt vroegtijdige waarschuwing op Lake George Hoe gaat het om uw licht op effect op de omgeving te laten?
Hoe gaat het om uw licht op effect op de omgeving te laten?
Hoofdlijnen
- Hoe begrijpen vogels 'buitenlandse' oproepen?
- Een gen heeft de basissequentie die begint met TCG GAC Cat CGAG B) Wat zou mRNA worden gevormd uit dit DNA?
- Waar worden lysosomen gevonden in een plantencel?
- De werkelijke genensamenstelling van een organisme is dat?
- Welk celtype wordt in de grootste overvloed de kiemcentra gevonden?
- Populair hulpmiddel dat door biologen wordt gebruikt om ecosystemen te proeven?
- Coole ideeën voor een 3D-model van DNA
- Welke eiwitten en andere materialen van het ene deel van de cel naar het andere?
- Hoe wordt een grote holte of zak genoemd die in plantencellen van protozoën wordt aangetroffen en die gedeeltelijk verteerd voedsel bevat?
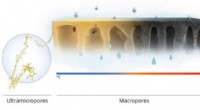
- Brandmembranen voor moleculair zeven
- Wetenschappers gaan diep om de eigenschappen van perovskiet te kwantificeren

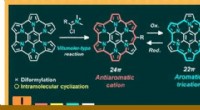
- In stikstof ingebedde polycyclische verbinding met sterke anti-aromaticiteit en stabiliteit
- Eenvoudige entropieën voor gecompliceerde moleculen

- Upcycling van plastic afval tot hoogwaardige mechanische smeermiddelen

 Ropen alle planeten in dezelfde richting?
Ropen alle planeten in dezelfde richting?  Waarom werknemers in kleine bedrijven kunnen worstelen met geestelijke gezondheid en 'presenteïsme'
Waarom werknemers in kleine bedrijven kunnen worstelen met geestelijke gezondheid en 'presenteïsme'  Wetenschappers ontwerpen een nieuw niet-lineair circuit om schone energie te oogsten met behulp van grafeen
Wetenschappers ontwerpen een nieuw niet-lineair circuit om schone energie te oogsten met behulp van grafeen  Nanorobot voor transport van medicijnen in het lichaam
Nanorobot voor transport van medicijnen in het lichaam Hoe helpen plaattektoniek de aanwezigheid van unieke diersoorten op continenten zoals Australië te verklaren?
Hoe helpen plaattektoniek de aanwezigheid van unieke diersoorten op continenten zoals Australië te verklaren?  Wat is EMF in de natuurkunde?
Wat is EMF in de natuurkunde?  Waarom hopen wetenschappers een manier te ontdekken om de rijping te versnellen?
Waarom hopen wetenschappers een manier te ontdekken om de rijping te versnellen?  Toegang tot energie voor iedereen in Afrika bezuiden de Sahara
Toegang tot energie voor iedereen in Afrika bezuiden de Sahara
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

