
Wetenschap
Is chloor trifluoride CIF3 polair of niet -polair?
* Moleculaire geometrie: CLF3 heeft een T-vormige moleculaire geometrie. Dit betekent dat het centrale chlooratoom drie fluoratomen heeft verbonden en één eenzijdig paar elektronen.
* elektronegativiteit: Fluor is veel elektronegatiefer dan chloor. Dit betekent dat de fluoratomen de elektronendichtheid naar zichzelf trekken, waardoor een gedeeltelijke negatieve lading (A-) op de fluoratomen en een gedeeltelijke positieve lading (A+) op het chlooratoom ontstaat.
* asymmetrie: De T-vormige geometrie en de ongelijke verdeling van elektronendichtheid als gevolg van elektronegativiteitsverschillen creëren een asymmetrisch molecuul. Deze asymmetrie betekent dat de dipoolmomenten (vectoren die de richting van de gedeeltelijke ladingen vertegenwoordigen) elkaar niet annuleren.
Daarom heeft CLF3 een netto dipoolmoment en wordt het als een polair molecuul beschouwd.
 Wat is het veiligste zuur of alkali?
Wat is het veiligste zuur of alkali?  Welke kleur verandert kopersulfaat de universele indicator?
Welke kleur verandert kopersulfaat de universele indicator?  Machine learning gebruiken om veelbelovende polymeermembranen te identificeren
Machine learning gebruiken om veelbelovende polymeermembranen te identificeren Specifieke ioneneffecten gericht op aerogels van edelmetaal
Specifieke ioneneffecten gericht op aerogels van edelmetaal Supercomputers simuleren nieuwe paden voor mogelijke behandeling van RNA-virussen
Supercomputers simuleren nieuwe paden voor mogelijke behandeling van RNA-virussen
 Het is geweldig dat Blue Planet II hard aandringt op plasticvervuiling in de oceanen - maar gebruik alstublieft feiten, geen vermoeden
Het is geweldig dat Blue Planet II hard aandringt op plasticvervuiling in de oceanen - maar gebruik alstublieft feiten, geen vermoeden Onderzoek naar oceaanverzuring pleit sterk voor beperking van klimaatverandering
Onderzoek naar oceaanverzuring pleit sterk voor beperking van klimaatverandering De plasticafvalcrisis is een kans voor de VS om thuis serieus te gaan recyclen
De plasticafvalcrisis is een kans voor de VS om thuis serieus te gaan recyclen Wetenschappers stellen verklaring voor nachtelijke hemelgloed van STEVE . voor
Wetenschappers stellen verklaring voor nachtelijke hemelgloed van STEVE . voor Hoe voedselkeuzes de planeet kunnen helpen
Hoe voedselkeuzes de planeet kunnen helpen
Hoofdlijnen
- Reusachtige 200 jaar oude cactus omgevallen door hevige regen in de VS
- Onderzoek toont aan hoe de chemische eigenschappen van RNA-moleculen het oorspronkelijke leven hadden kunnen vergemakkelijken
- Welk doel diende suiker voor de gist?
- Onderzoekers onderzoeken de impact van verhoogde CO₂-concentratie op subtropische bomen
- Nieuw onderzoek wijst uit dat walvistanden na het midden van de dracht nog steeds aanwezig zijn, wat enigszins verrassend is
- Wat is de functie van Cilia in de buurt van de mond?
- Mutualisme is een soort symbiotische relatie waarin wat er gebeurt tussen twee organismen?
- Wat is een psyllidvector?
- Wat zou er met een voedselketen gebeuren als de populatie van één organisme zou toenemen?
- Kunstmatige bladeren uit het lab de lucht in verplaatsen

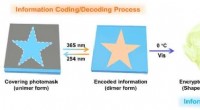
- Nieuwe fluorescerende organohydrogel voorgesteld om dubbele informatie-encryptie te bereiken
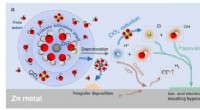
- Gehydrateerde eutectische elektrolyten helpen de prestaties van waterige zinkbatterijen te verbeteren
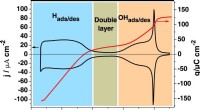
- Nieuw begrip van de belangrijkste brandstofcelkatalysator
- Een licht schijnen op de kwestie van wijnfraude

 Video:Zou kanker onze oudste voorouder kunnen zijn?
Video:Zou kanker onze oudste voorouder kunnen zijn?  Wat is energie van warmte genoemd?
Wat is energie van warmte genoemd?  High School PI Day-projecten
High School PI Day-projecten  Walmart werkt samen met Google voor boodschappen via spraak
Walmart werkt samen met Google voor boodschappen via spraak Welk mineraal bevat ijzer heeft een metalen glans is moeilijk en dezelfde kleurstreak?
Welk mineraal bevat ijzer heeft een metalen glans is moeilijk en dezelfde kleurstreak?  Moleculaire additieven verbeteren de mechanische eigenschappen van organisch zonnecelmateriaal
Moleculaire additieven verbeteren de mechanische eigenschappen van organisch zonnecelmateriaal Welk type textuur heeft extrusieve rots zoals basalt?
Welk type textuur heeft extrusieve rots zoals basalt?  Astronomen draaien de klok terug om de tijdlijn van een stellaire explosie te bepalen
Astronomen draaien de klok terug om de tijdlijn van een stellaire explosie te bepalen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

