
Wetenschap
Natriumacetaatdissociatie:vergelijking en uitleg
NaC₂H₃O₂ (aq) ⇌ Na⁺ (aq) + C₂H₃O₂⁻ (aq)
Dit is wat de vergelijking betekent:
* NaC₂H₃O₂ (aq): Natriumacetaat opgelost in water (waterige oplossing).
* Na⁺ (aq): Natriumkation (positief geladen ion) opgelost in water.
* C₂H₃O₂⁻ (aq): Acetaatanion (negatief geladen ion) opgelost in water.
* ⇌: Deze dubbele pijl geeft aan dat de reactie een evenwicht is. Dit betekent dat de reactie in beide richtingen kan verlopen, waarbij natriumacetaat dissocieert in zijn ionen en ionen combineren om natriumacetaat te vormen.
Belangrijkste punten:
* Natriumacetaat is een sterke elektrolyt, wat betekent dat het volledig in ionen uiteenvalt wanneer het in water wordt opgelost.
* Het acetaation (C₂H₃O₂⁻) is de geconjugeerde base van azijnzuur (CH₃COOH), een zwak zuur.
* De oplossing van natriumacetaat zal enigszins basisch zijn vanwege de hydrolyse van acetaationen, die protonen uit watermoleculen kunnen accepteren.
 Plastic microvezels voor het eerst gevonden in ontlasting van wilde dieren van Zuid-Amerikaanse pelsrobben
Plastic microvezels voor het eerst gevonden in ontlasting van wilde dieren van Zuid-Amerikaanse pelsrobben Een vurig verleden werpt nieuw licht op de toekomst van de wereldwijde klimaatverandering
Een vurig verleden werpt nieuw licht op de toekomst van de wereldwijde klimaatverandering Wat eeuwenoud stuifmeel ons vertelt over toekomstige klimaatverandering
Wat eeuwenoud stuifmeel ons vertelt over toekomstige klimaatverandering  Om nutsbedrijven te helpen, onderzoekers zoeken oude overstromingen in de buurt van Tennessee River
Om nutsbedrijven te helpen, onderzoekers zoeken oude overstromingen in de buurt van Tennessee River Inzicht in alternatieve redenen om klimaatverandering te ontkennen, kan helpen om de kloof te overbruggen
Inzicht in alternatieve redenen om klimaatverandering te ontkennen, kan helpen om de kloof te overbruggen
Hoofdlijnen
- Welke soorten klinische monsters kunnen een gemengde flora opleveren in bacteriële culturen?
- Onderzoekers ontwikkelen een model om te laten zien hoe bacteriën groeien in sanitaire systemen
- Welk deel van het DNA vormt buiten ladderstructuren?
- Wat is het verschil tussen een endotherme organisme en ectothermisch organisme?
- Welke soorten organismen zijn docomposers?
- Hoe resulteren transcriptie en translatie in de expressie van genen?
- Latijn en Grieks:de talen van de wetenschappelijke nomenclatuur
- Wat zijn de veelgebruikte microbiële bacteriën in de biotechnologie?
- Hoe muizen de beste ontsnappingsroute kiezen
- Waarom de pH van gedestilleerd water onder de 7 daalt:de rol van atmosferische CO₂
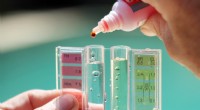
- Een eenvoudig recept voor MRI-contrasten tot vier keer hoger
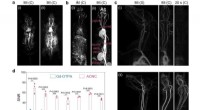
- Chemicaliën kunnen hun identiteit veranderen, dankzij de vloeistoffen waar ze zich bevinden
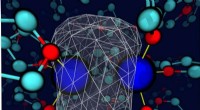
- Onderzoekers ontwikkelen goedkope, drop-on-demand printtechniek

- Een unieke geleidende toestand onder UV-straling

 Wat is een complex koolhyraat dat plantenstelen en wortels versterkt?
Wat is een complex koolhyraat dat plantenstelen en wortels versterkt?  Grafeen en andere koolstofnanomaterialen kunnen schaarse metalen vervangen
Grafeen en andere koolstofnanomaterialen kunnen schaarse metalen vervangen Sterren in een baan om superzware zwarte gaten laten zien dat Einstein weer gelijk had
Sterren in een baan om superzware zwarte gaten laten zien dat Einstein weer gelijk had Wat is de elektronenwoede?
Wat is de elektronenwoede?  Anythin dat verandering veroorzaakt, moet energie hebben. T of f?
Anythin dat verandering veroorzaakt, moet energie hebben. T of f?  Een 70-jarige benadering van het voorspellen van de microstructuur van materialen weerleggen
Een 70-jarige benadering van het voorspellen van de microstructuur van materialen weerleggen Alleen oesters eten in maanden met een 'r'? De vuistregel is minstens 4.000 jaar oud
Alleen oesters eten in maanden met een 'r'? De vuistregel is minstens 4.000 jaar oud  Slibstroom volgen voor betere afvalwaterzuivering en meer biogas
Slibstroom volgen voor betere afvalwaterzuivering en meer biogas
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

