
Wetenschap
Neutralisatiereacties in de chemie:definitie, proces en voorbeelden
Neutralisatie in de chemie:een evenwichtsoefening
Neutralisatie in de chemie verwijst naar de reactie tussen een zuur en een basis , resulterend in de vorming van zout en water . Deze reactie gaat vaak gepaard met het vrijkomen van warmte, waardoor het een exotherme reactie wordt .
Hier is een overzicht:
* Zuur: Een stof die waterstofionen (H+) in oplossing afstaat. Voorbeelden hiervan zijn zoutzuur (HCl) en zwavelzuur (H2SO4).
* Basis: Een stof die waterstofionen (H+) in oplossing accepteert. Voorbeelden zijn onder meer natriumhydroxide (NaOH) en kaliumhydroxide (KOH).
* Zout: Een ionische verbinding die wordt gevormd door de reactie van een zuur en een base. Zouten kunnen neutraal, zuur of basisch zijn, afhankelijk van de sterkte van het betrokken zuur en de base.
* Water: Gevormd door de combinatie van waterstofionen (H+) uit het zuur en hydroxide-ionen (OH-) uit de base.
De vergelijking:
De algemene vergelijking voor neutralisatie is:
Zuur + Base → Zout + Water
Voorbeeld:
De neutralisatiereactie tussen zoutzuur (HCl) en natriumhydroxide (NaOH) produceert natriumchloride (NaCl) en water (H2O).
HCl (zuur) + NaOH (base) → NaCl (zout) + H2O (water)
Belang:
Neutralisatiereacties zijn cruciaal bij verschillende toepassingen, waaronder:
* pH-controle: Neutralisatie wordt gebruikt om de pH van oplossingen aan te passen, zoals bij afvalwaterzuivering en industriële processen.
* Opruiming van zure lekkage: Neutralisatiemiddelen worden gebruikt om gemorste zuren te neutraliseren, waardoor schade aan mens en milieu wordt voorkomen.
* Titratie: Neutralisatiereacties worden bij titratie gebruikt om de concentratie van een onbekend zuur of onbekende base te bepalen.
* Geneeskunde: Antacida, die maagzuur neutraliseren, zijn een bekend voorbeeld van neutralisatie in de geneeskunde.
Belangrijkste concepten:
* pH: Een maatstaf voor de zuurgraad of alkaliteit, waarbij een pH van 7 neutraal is.
* Sterk zuur/base: Een zuur of base die in oplossing volledig dissocieert, waarbij al zijn H+ of OH-ionen vrijkomen.
* Zwak zuur/base: Een zuur of base die in oplossing slechts gedeeltelijk dissocieert, waarbij slechts een deel van zijn H+- of OH--ionen vrijkomt.
* Neutralisatiepunt: Het punt in een titratie waarop het zuur en de base volledig zijn geneutraliseerd, wat resulteert in een neutrale pH van 7.
Neutralisatie is een fundamenteel concept in de chemie dat het gedrag van zuren en basen en hun interacties helpt verklaren. Het begrijpen van neutralisatiereacties is essentieel voor verschillende wetenschappelijke en praktische toepassingen.
 Een materiaalwetenschappelijke benadering van de bestrijding van het coronavirus
Een materiaalwetenschappelijke benadering van de bestrijding van het coronavirus Elektrochemische synthese van formiaat uit koolstofdioxide met behulp van een tin/gereduceerde grafeenoxidekatalysator
Elektrochemische synthese van formiaat uit koolstofdioxide met behulp van een tin/gereduceerde grafeenoxidekatalysator Welk gas wordt gebruikt om bruis in koolzuurhoudende dranken te doen?
Welk gas wordt gebruikt om bruis in koolzuurhoudende dranken te doen?  Is zand een verbinding of een heterogene mengsel van een element -homogeen mengsel?
Is zand een verbinding of een heterogene mengsel van een element -homogeen mengsel?  Uit welke stoffen bestaat een covalente stof?
Uit welke stoffen bestaat een covalente stof?
Hoofdlijnen
- Lijst van nummerchromosomen aanwezig in verschillende planten en dieren?
- Welke activiteit zou op het gebied van biololgy zijn?
- Wat is de beste term om correctheid in een hypothese te beschrijven?
- Hoe reproduceert Gladiolus zich?
- Waar wordt biotechnologie gebruikt?
- Wat zijn allelparen van een organisme?
- Dolfijnengezondheidscontrole toont toestand van onze oceanen
- Welk proces is de eerste stap bij het maken van een eiwit van DNA -instructie?
- Waarom worden soms gebruikt om chromosomen weer te geven?
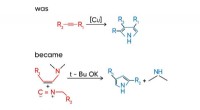
- Chemici stellen een nieuwe methode voor voor de synthese van pyrrolen
- Nieuwe watersplitsingskatalysator kan het gemakkelijker maken om zonnebrandstof te genereren

- Fidget spinner als centrifuge scheidt bloedplasma
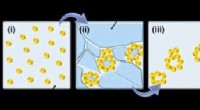
- Gestructureerde materialen op meerdere schalen voor elektrokatalyse en foto-elektrokatalyse
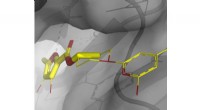
- Op fragmenten gebaseerde benaderingen gebruiken om nieuwe antibiotica te ontdekken
 Wat is de leidingrichting als de zwaartekracht gelijk is aan elektrostatische kracht?
Wat is de leidingrichting als de zwaartekracht gelijk is aan elektrostatische kracht?  Wat u moet weten over de laatste uitbraak van vogelgriep in de VS
Wat u moet weten over de laatste uitbraak van vogelgriep in de VS  Voorbeeld van technologie was gerelateerd aan natuurkunde?
Voorbeeld van technologie was gerelateerd aan natuurkunde?  Vuurtornado's uitgelegd
Vuurtornado's uitgelegd Wat is 63 kg in stenen?
Wat is 63 kg in stenen?  Meer van de Chinese bevolking zal worden blootgesteld aan hittegolven
Meer van de Chinese bevolking zal worden blootgesteld aan hittegolven Zelfaangedreven alarm bestrijdt bosbranden, bewaakt de omgeving
Zelfaangedreven alarm bestrijdt bosbranden, bewaakt de omgeving Grote fossiele ontdekking onthult eindelijk de oorsprong van Welshe draken
Grote fossiele ontdekking onthult eindelijk de oorsprong van Welshe draken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

