
Wetenschap
Lithium en Francium:hun vergelijkbare eigenschappen begrijpen - Periodiek Systeem
* Elektronenconfiguratie: Zowel Lithium als Francium hebben één valentie-elektron (elektron in de buitenste schil). Dit enkele elektron gaat gemakkelijk verloren, waardoor ze zeer reactief zijn en graag kationen vormen met een lading van +1.
* Atomische grootte: Hoewel Francium veel groter is dan lithium, ondervindt hun buitenste elektron vergelijkbare afschermingseffecten van de binnenste elektronen. Dit betekent dat het valentie-elektron in beide elementen zich relatief ver van de kern bevindt en losjes gebonden is.
* Elektropositiviteit: Vanwege hun lage ionisatie-energieën (de energie die nodig is om een elektron te verwijderen), zijn lithium en francium zeer elektropositief. Dit betekent dat ze gemakkelijk elektronen verliezen en positieve ionen vormen, wat bijdraagt aan hun reactiviteit.
* Reactiviteit: Als alkalimetalen zijn ze uiterst reactief, vooral met water. Deze reactiviteit neemt toe naarmate je verder in de groep komt, waardoor Francium de meest reactieve van allemaal is.
Samengevat: Hun vergelijkbare elektronenconfiguraties, atomaire afmetingen en elektropositiviteit vanwege hun gedeelde positie in Groep 1 van het periodiek systeem leiden tot de vergelijkbare chemische eigenschappen van Lithium en Francium.
 Waar is kwik te vinden?
Waar is kwik te vinden?  Welk homeostatisch proces wordt gekenmerkt door de diffusie van watermoleculen?
Welk homeostatisch proces wordt gekenmerkt door de diffusie van watermoleculen?  Waarom veranderen hydraten van kleur wanneer ze worden verwarmd?
Waarom veranderen hydraten van kleur wanneer ze worden verwarmd?  Noem het gas dat van nature voorkomt in lucht en schermen schadelijke stralen uit de zon?
Noem het gas dat van nature voorkomt in lucht en schermen schadelijke stralen uit de zon?  Bereken de kookpunthoogte van een zoutwateroplossing die 3,40 g NaCl opgelost in 148 ml water bevat?
Bereken de kookpunthoogte van een zoutwateroplossing die 3,40 g NaCl opgelost in 148 ml water bevat?
Hoofdlijnen
- Botsing van de rivierkreeft:waarom Amerikanen winnen
- Wat is de medische term die betekent gedraaide ketens van bessenvormige bacteriën?
- Wat veroorzaakt ziekte-uitbraken?
- Verborgen spelers in de klimaatverandering:hoe microscopische eiwitten onze toekomst kunnen vormgeven
- Wat is celtheorie en wie is de wetenschapper die theorie vestigt?
- Groep van micro -organismen gecomponeerd alleen erfelijk materiaal gewikkeld in een eiwitbedekking?
- Zijn er dieren immuun voor prionziekten?
- Het richten op een enkel eiwit kan een breed scala aan virussen behandelen
- Wat zijn de drie belangrijkste bewijsgebieden voor evolutie?
- Wetenschappers ontwikkelen sondes die zijn ontworpen om de fysieke krachten in levende cellen te onthullen; een wereldprimeur

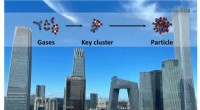
- Verborgen zuur-base clusters zorgen voor snelle vorming van atmosferische ultrafijne deeltjes
- Eenvoudige watertest kan verlammende botziekte voorkomen

- Door genetisch materiaal op te sporen, snelle sensor heeft potentieel gebruik als klinisch hulpmiddel
- Combinatorische strategie met hoge doorvoer voorgesteld om reactiekatalysatoren voor waterstofontwikkeling te screenen

 Hoe wordt helium dat geproduceerd door de omzetting van waterstof in energie gerelateerd aan zonne -kern?
Hoe wordt helium dat geproduceerd door de omzetting van waterstof in energie gerelateerd aan zonne -kern?  Wat is de samenstelling van algen?
Wat is de samenstelling van algen?  Wat is de relatie waarin ten minste één soort voordelen?
Wat is de relatie waarin ten minste één soort voordelen?  Is er een aanpassing voor de spijsvertering?
Is er een aanpassing voor de spijsvertering?  Wat de droogte in Kaapstad andere steden kan leren over klimaatadaptatie
Wat de droogte in Kaapstad andere steden kan leren over klimaatadaptatie Als je over een aardbeving vloog,
Als je over een aardbeving vloog,  Wat heeft twee of meer paden waar elektriciteit kan stromen?
Wat heeft twee of meer paden waar elektriciteit kan stromen?  Waarom klimaatverandering belangrijk is
Waarom klimaatverandering belangrijk is
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

