
Wetenschap
Bereken de pH van een 3% azijnzuuroplossing:een stapsgewijze handleiding
1. Begrijp de concepten
* Azijnzuur (CH3COOH): Een zwak zuur, wat betekent dat het niet volledig ioniseert in water.
* pH: Een maatstaf voor de zuurgraad of alkaliteit van een oplossing. Een lagere pH duidt op een sterker zuur.
* Ka: De zuurdissociatieconstante, die de sterkte van een zuur aangeeft. Voor azijnzuur geldt Ka =1,8 x 10^-5.
2. Bereken de molariteit van de oplossing
* 3% azijnzuur betekent 3 g azijnzuur per 100 ml oplossing.
* Gramen omrekenen naar mol:
* Molaire massa azijnzuur (CH3COOH) =60,05 g/mol
* Mol azijnzuur =(3 g) / (60,05 g/mol) =0,05 mol
* ML omzetten naar L: 100 ml =0,1 liter
* Bereken de molariteit (M):
* Molariteit =(mol opgeloste stof) / (volume oplossing in liters)
* Molariteit =(0,05 mol) / (0,1 L) =0,5 M
3. Stel de evenwichtsexpressie in
Azijnzuur ioniseert in water volgens het volgende evenwicht:
CH3COOH(aq) ⇌ H+(aq) + CH3COO-(aq)
* Initiële concentraties:
* [CH3COOH] =0,5 M
* [H+] =0 (aanvankelijk)
* [CH3COO-] =0 (aanvankelijk)
* Verandering in concentraties:
* -x (voor CH3COOH)
* +x (voor H+)
* +x (voor CH3COO-)
* Evenwichtsconcentraties:
* [CH3COOH] =0,5 - x
* [H+] =x
* [CH3COO-] =x
4. Gebruik de Ka-expressie om [H+] op te lossen
Ka =[H+][CH3COO-] / [CH3COOH]
1,8 x 10^-5 =(x)(x) / (0,5 - x)
5. Vereenvoudig de vergelijking (aanname)
Omdat Ka klein is, kunnen we aannemen dat x veel kleiner is dan 0,5. Hierdoor kunnen we de vergelijking vereenvoudigen:
1,8x10^-5 ≈x^2 / 0,5
6. Los op voor x (wat gelijk is aan [H+])
* x^2 =9x10^-6
* x =√(9 x 10^-6) =3 x 10^-3 M
7. Bereken de pH
pH =-log[H+]
pH =-log(3 x 10^-3)
pH ≈ 2,52
Daarom is de pH van een 3% azijnzuuroplossing ongeveer 2,52.
 Hoe we de vroegste glasproductie ten zuiden van de Sahara vonden, en wat het betekent
Hoe we de vroegste glasproductie ten zuiden van de Sahara vonden, en wat het betekent Wat gebeurt er met de temperatuur van een stof tijdens faseverandering?
Wat gebeurt er met de temperatuur van een stof tijdens faseverandering?  Wat gebeurt er als zoutzuur op een cu-plaat wordt gegoten?
Wat gebeurt er als zoutzuur op een cu-plaat wordt gegoten?  Goedkoop, energiezuinige aanpak voor de behandeling van met zware metalen verontreinigd water
Goedkoop, energiezuinige aanpak voor de behandeling van met zware metalen verontreinigd water Kun je van water in poeder veranderen?
Kun je van water in poeder veranderen?
 Wat is een Imprint Fossil?
Wat is een Imprint Fossil?  Supercharged onweersbuien:hebben we onderschat hoe klimaatverandering extreme regen en overstromingen veroorzaakt?
Supercharged onweersbuien:hebben we onderschat hoe klimaatverandering extreme regen en overstromingen veroorzaakt?  Is deze geit de GEIT? Jongen met lange oren verovert Pakistan stormenderhand
Is deze geit de GEIT? Jongen met lange oren verovert Pakistan stormenderhand  Onderzoek helpt bij het vaststellen wat soorten kwetsbaar maakt voor veranderingen in het milieu
Onderzoek helpt bij het vaststellen wat soorten kwetsbaar maakt voor veranderingen in het milieu  Veranderingen in brandactiviteit bedreigen meer dan 4, 400 soorten wereldwijd
Veranderingen in brandactiviteit bedreigen meer dan 4, 400 soorten wereldwijd
Hoofdlijnen
- Wat is functie van meiose?
- Wat is een bacterie die zuurstof nodig heeft?
- Wat zijn lobben in een kern?
- Onderzoekers werpen licht op hoe een belangrijk ingrediënt voor leven zich in de ruimte kan vormen
- Wat is een Darwin Delgado?
- Hoe zijn chloroplasten en mitochondriën vergelijkbaar met bacteriën?
- Welke celorganellen bevat materialen?
- Wat is de wetenschappelijke naam of taxonomische classificatie van giftige plantenkoffie senna?
- Hoe classificeren wetenschappers archeebacteriën?
- Supercomputing verbetert de conversie van biomassabrandstof
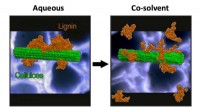
- Kooldioxide omzetten in waardevolle producten

- In de brandstofcel:beeldvormingsmethode belooft industrieel inzicht

- Keramische membranen scheiden kleine organische moleculen met een molecuulmassa van 200 Dalton

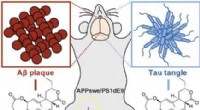
- Wortelbacterie om Alzheimer te bestrijden:Rhizolutin dissocieert bèta- en tau-aggregaten
 Totaal verliest bod voor belastingvoordeel palmolie
Totaal verliest bod voor belastingvoordeel palmolie Bodemgegevens onthullen geheimen in het oude Israël
Bodemgegevens onthullen geheimen in het oude Israël Wat is een kleine organismen met één cellen die geen kernen bevatten?
Wat is een kleine organismen met één cellen die geen kernen bevatten?  Wat betekent het woord niche in het ecosysteem?
Wat betekent het woord niche in het ecosysteem?  Wat is een bocht in Crustal Rock?
Wat is een bocht in Crustal Rock?  Waarom werken enzymen in tegengestelde detecties replicatie?
Waarom werken enzymen in tegengestelde detecties replicatie?  Welke kleur van regenboog heeft de hoogste energie?
Welke kleur van regenboog heeft de hoogste energie?  De weg naar duurzame energie verlichten
De weg naar duurzame energie verlichten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

